Hydrogenbinding vs. kovalente bindinger:Forstå forskellen
* Kovalente bindinger involverer deling af elektroner mellem atomer. Disse er stærke bindinger, der holder atomer sammen i et molekyle.
* Brintbindinger er en type intermolekylær kraft, hvilket betyder, at de forekommer mellem molekyler, ikke inden i dem. De opstår fra tiltrækningen mellem et let positivt brintatom (bundet til et meget elektronegativt atom som oxygen eller nitrogen) og et ensomt elektronpar på et andet elektronegativt atom.
Mens hydrogenbindinger er relativt stærke sammenlignet med andre intermolekylære kræfter (som Van der Waals-kræfter), er de væsentligt svagere end kovalente bindinger.
Her er en tabel, der sammenligner deres styrker:
| Obligationstype | Styrke (kJ/mol) |
|---|---|
| Kovalent binding | 100-1000 |
| Hydrogenbinding | 5-40 |
| Van der Waals styrker | 0,1-5 |
Opsummering:
* Hydrogenbinding er en intermolekylær kraft, der er svagere end kovalent binding.
* Hydrogenbindinger er afgørende for mange biologiske og kemiske processer, herunder vands unikke egenskaber, proteinfoldning og DNA-struktur.
 Varme artikler
Varme artikler
-
 Fuglefjer inspirerer forskere til at producere levende nye farverBioinspireret lyst strukturelt farvet kolloidalt amorft array forstærket af styring af tykkelse og sort baggrund. Kredit:Yukikazu Takeoka Et forskergruppe ledet af Nagoya Universitet efterligner f
Fuglefjer inspirerer forskere til at producere levende nye farverBioinspireret lyst strukturelt farvet kolloidalt amorft array forstærket af styring af tykkelse og sort baggrund. Kredit:Yukikazu Takeoka Et forskergruppe ledet af Nagoya Universitet efterligner f -
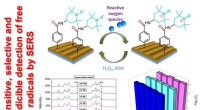 Forskere skaber sensorer med fælder til frie radikalerSensor drift diagram. Kredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University og partnere fra Tjekkiet og Frankrig har designet ekstremt følsomme sensorer til frie iltholdi
Forskere skaber sensorer med fælder til frie radikalerSensor drift diagram. Kredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University og partnere fra Tjekkiet og Frankrig har designet ekstremt følsomme sensorer til frie iltholdi -
 Fysikere udvikler en ny metode til at identificere antibiotika-resistente bakterierHolder med prøver af mykobakteriestammer med forskellig antibiotikaresistens. Kredit:Andrey Zyubin Et hold fysikere fra Immanuel Kant Baltic State University har foreslået en metode til at identif
Fysikere udvikler en ny metode til at identificere antibiotika-resistente bakterierHolder med prøver af mykobakteriestammer med forskellig antibiotikaresistens. Kredit:Andrey Zyubin Et hold fysikere fra Immanuel Kant Baltic State University har foreslået en metode til at identif -
 Forskere afslører ny dobbelt-roaming-mekanisme i kemisk reaktion3D polært plot for produktets translationelle energi og vinkelfordelinger. Kredit:FU Yanlin Roaming, en ny mekanisme i reaktionsdynamik, beskriver en usædvanlig vej, der er ret forskellig fra den
Forskere afslører ny dobbelt-roaming-mekanisme i kemisk reaktion3D polært plot for produktets translationelle energi og vinkelfordelinger. Kredit:FU Yanlin Roaming, en ny mekanisme i reaktionsdynamik, beskriver en usædvanlig vej, der er ret forskellig fra den
- Hvilken organelle er mest rigelig i sædcellen?
- En rumprobe på overfladen af Mars sender et radiosignal tilbage til Jorden afstand 7,03 x 107 km.…
- Traditionelle landbrugsmetoder i et tørt klima
- Undersøgelse af 90 dyrs lårknogler afslører, hvordan de effektivt kan bære byrder
- Hvad er momentum målet for?
- Er nukleare reaktioner en ikke -vedvarende energikilde?


