Spontane reaktioner i kemi:Definition &nøglekarakteristika
Her er en opdeling:
Spontan reaktion:
* Fordelagtigt: Produkterne er mere stabile end reaktanterne.
* Energi frigivet: Reaktionen frigiver energi (eksotermisk).
* Entropien stiger: Produkterne er mere uordnede end reaktanterne.
* Betyder ikke hurtigt: Reaktionen kan ske meget langsomt, selvom den er spontan.
Ikke-spontan reaktion:
* Ugunstig: Reaktanterne er mere stabile end produkterne.
* Energi påkrævet: Reaktionen kræver energitilførsel (endotermisk) for at forekomme.
* Entropien falder: Produkterne er mere ordnede end reaktanterne.
* Kræver eksternt input: Kommer ikke til at ske af sig selv.
Nøglepunkt:
En spontan reaktion er ikke nødvendigvis en hurtig reaktion. Faktorer som aktiveringsenergi, temperatur og katalysatorer kan påvirke hastigheden af en reaktion, uanset om den er spontan eller ej.
Eksempel:
* Spontan: Rustning af jern (Fe + O₂ → Fe₂O₃) er spontan ved stuetemperatur, men processen er langsom.
* Ikke-spontan: Nedbrydningen af vand til hydrogen og oxygen (2H2O → 2H2 + O2) er ikke-spontan under standardbetingelser. Det kræver elektrisk energitilførsel for at ske.
Opsummering:
Spontane reaktioner er dem, der sker naturligt, frigiver energi og øger uorden. Mens spontanitet indebærer en reaktion *kan* ske, fortæller den os ikke *hvor hurtigt* den vil ske.
 Varme artikler
Varme artikler
-
 Skab en bedre paryk med kemiHår belagt med en nanokomposit (til venstre) ved hjælp af Langmuir-Blodgett-teknikken genererer meget mindre statisk elektricitet end ubehandlede hår (højre). Kredit:Tilpasset fra ACS Applied Material
Skab en bedre paryk med kemiHår belagt med en nanokomposit (til venstre) ved hjælp af Langmuir-Blodgett-teknikken genererer meget mindre statisk elektricitet end ubehandlede hår (højre). Kredit:Tilpasset fra ACS Applied Material -
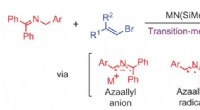 Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk
Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk -
 Lysfarvet 3D-print ved hjælp af flydende krystallera) Oversigt over det centrale element i direkte blækskrivning (DIW):sprøjten med mikrodyse. Angivet er placeringen af blækket, varmekappen (til temperaturstyret DIW), mikrodysen og det trykte objekt
Lysfarvet 3D-print ved hjælp af flydende krystallera) Oversigt over det centrale element i direkte blækskrivning (DIW):sprøjten med mikrodyse. Angivet er placeringen af blækket, varmekappen (til temperaturstyret DIW), mikrodysen og det trykte objekt -
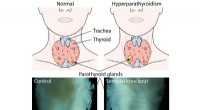 Opdagelse af signalprotein kan føre til lægemiddelbaserede terapier til behandling af hyperparathy…Fire små biskjoldbruskkirtler placeret i nakken bag den større skjoldbruskkirtel er ansvarlige for at styre sunde blodcalciumniveauer. Primær hyperparatyreoidisme er præget af overdreven parathyreoide
Opdagelse af signalprotein kan føre til lægemiddelbaserede terapier til behandling af hyperparathy…Fire små biskjoldbruskkirtler placeret i nakken bag den større skjoldbruskkirtel er ansvarlige for at styre sunde blodcalciumniveauer. Primær hyperparatyreoidisme er præget af overdreven parathyreoide
- Nye Interstellar Boundary Explorer-data viser, at heliosfærens lange teoretiserede buestød ikke ek…
- Hvilken type energi rejser fra brødristeren?
- Nyt kort viser, hvordan klimaændringer påvirker dit samfund og dets sårbarhed over for vejret
- Hvor lang er en måneaften?
- Forskere bruger SERS-teknologi til nøjagtigt at overvåge enkelt-molekylets diffusionsadfærd
- Hvorfor er det fysiske miljø vigtigt for levende organismer?


