Forståelse af kovalente bindinger:Dannelse, struktur og deling
1. Atomstruktur:
* Elektroner: Atomer har negativt ladede elektroner, der kredser om deres kerne. Elektroner bor i energiniveauer kaldet skaller. Den yderste skal, kaldet valensskallen, er afgørende for bindingen.
* Stabilitet: Atomer stræber efter en stabil konfiguration, typisk med en fuld ydre skal (normalt 8 elektroner, kendt som oktetreglen).
2. Deling af elektroner:
* Når atomer med ufuldstændige valensskaller mødes, kan de dele elektroner for at opnå en stabil konfiguration.
* Denne deling resulterer i en kovalent binding , hvor de delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen.
3. Typer af kovalente bindinger:
* Single Bond: Et par elektroner er delt mellem to atomer.
* Dobbeltbinding: To par elektroner er delt mellem to atomer.
* Trippelbinding: Tre par elektroner er delt mellem to atomer.
Eksempel:Vand (H₂O)
* Oxygen har 6 elektroner i sin ydre skal og har brug for 2 mere for at opnå stabilitet.
* Hvert brintatom har 1 elektron i sin ydre skal og har brug for 1 mere.
* Oxygen deler en elektron med hvert brintatom og danner to enkelt kovalente bindinger. Dette fuldender de ydre skaller af alle involverede atomer, hvilket gør molekylet stabilt.
Nøgleegenskaber for kovalente bindinger:
* Stærk: Kovalente bindinger er stærke og kræver betydelig energi for at bryde.
* Retningsbestemt: De delte elektroner er lokaliseret mellem de bundne atomer, hvilket skaber en specifik retningsbestemthed.
* Ikke-polær vs. Polar:
* Ikke-polær: Elektroner deles ligeligt mellem atomer med lignende elektronegativitet.
* Polar: Elektroner deles ulige mellem atomer med forskellig elektronegativitet, hvilket skaber partielle ladninger.
Sammenfattende dannes kovalente bindinger gennem deling af elektroner mellem atomer for at opnå en stabil konfiguration. Denne deling skaber en stærk og retningsbestemt binding, der spiller en afgørende rolle i dannelsen af molekyler.
 Varme artikler
Varme artikler
-
 Organiske metalskeletter lavet til at fungere som væskerEn udfordring for holdet var at få en krystallinsk MOF til at opføre sig som en porøs væske. Holdet opdagede, hvordan man modificerer overfladen af relativt store MOF-nanopartikler med passende kemi
Organiske metalskeletter lavet til at fungere som væskerEn udfordring for holdet var at få en krystallinsk MOF til at opføre sig som en porøs væske. Holdet opdagede, hvordan man modificerer overfladen af relativt store MOF-nanopartikler med passende kemi -
 Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio
Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio -
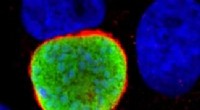 Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer
Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer -
 Undersøgelse viser potentiale for jordvenlig plasterstatningDen nye blanding af bioplast og gummi, der blev udtænkt af forskere i Ohio State, viste sig at være meget mere holdbar end bioplasten på egen hånd Credit:Ohio State University Stræben efter at hol
Undersøgelse viser potentiale for jordvenlig plasterstatningDen nye blanding af bioplast og gummi, der blev udtænkt af forskere i Ohio State, viste sig at være meget mere holdbar end bioplasten på egen hånd Credit:Ohio State University Stræben efter at hol
- Hvor kan jeg få et teleskop i Sims Social?
- Hvilke energiforandringer finder sted, når du ser et billede?
- En svamp, der skrumper i størrelse for bedre at inficere hjernen
- Hvilken klippe kan flyde som en væske?
- Regnen tæmmede Colorados sommersæson for skovbrande, men hvor længe holder heldet?
- Sådan fungerer Caterpillar rendegravere


