Forståelse af hydrogenperoxid pH:Faktorer og overvejelser
* Koncentration: pH-værdien af hydrogenperoxidopløsning afhænger i høj grad af dens koncentration. Mere koncentrerede opløsninger vil være mere sure.
* Dekomponering: Hydrogenperoxid nedbrydes til vand (H₂O) og oxygengas (O₂). Denne nedbrydningsproces fremskyndes af varme, lys og urenheder, som kan påvirke pH.
* Urenheder: pH-værdien af hydrogenperoxid kan påvirkes af urenheder, såsom syrer eller baser, der kan være til stede i opløsningen.
Du kan derfor ikke tildele en enkelt pH-værdi til hydrogenperoxid. For at bestemme pH-værdien skal du kende koncentrationen af den specifikke hydrogenperoxidopløsning, du arbejder med.
Generelle oplysninger:
* Fortyndede hydrogenperoxidopløsninger (3%): Disse er typisk let sure med en pH på omkring 6.
* Koncentrerede hydrogenperoxidopløsninger (30 % eller højere): Disse er mere sure og kan have en pH så lav som 2 eller 3.
Vigtig bemærkning: Det er afgørende at håndtere brintoverilte med omhu, især i koncentrerede former, da det kan være ætsende og forårsage hudirritation.
 Varme artikler
Varme artikler
-
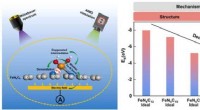 Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne
Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne -
 Bakterie-dræbende glas giver håb i kampen mod hospitalsinfektionerKredit:CC0 Public Domain Forskere ved Aston University har opdaget en teknik, der ligner middelalderfremstilling af farvet glas, der fuldstændigt kan udrydde de mest dødelige hospitalsinfektioner
Bakterie-dræbende glas giver håb i kampen mod hospitalsinfektionerKredit:CC0 Public Domain Forskere ved Aston University har opdaget en teknik, der ligner middelalderfremstilling af farvet glas, der fuldstændigt kan udrydde de mest dødelige hospitalsinfektioner -
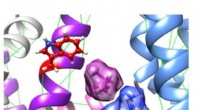 Forskere opdager molekylære mekanismer af gamle naturlægemidlerComputermodel af de to urtekomponenter, et isovalerinsyremolekyle (violet, øverst til venstre) og mallotoksin (blå, nederst til højre), optager tilstødende bindingssteder for synergistisk at aktivere
Forskere opdager molekylære mekanismer af gamle naturlægemidlerComputermodel af de to urtekomponenter, et isovalerinsyremolekyle (violet, øverst til venstre) og mallotoksin (blå, nederst til højre), optager tilstødende bindingssteder for synergistisk at aktivere -
 Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m
Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m
- Hvor mange meter er 150 cm?
- Hvorfor er det svært at stoppe med at rulle en bold?
- Hvilken lov siger, at energi aldrig opnås eller tabt?
- Hvorfor kan et bevægende objekt ikke komme til at stoppe øjeblikkeligt?
- Hjælper med at forbedre medicinsk billedanalyse med dyb læring
- Hvilket instrument kan bruges til at sammenligne masserne af to objekter?


