Geminale dioler:Forståelse af deres ustabilitet og dehydrering til ketoner/aldehyder
1. Sterisk hindring: De to hydroxylgrupper på det samme carbonatom er voluminøse og oplever betydelig sterisk hindring. Denne trængsel gør molekylet ustabilt.
2. Elektron-elektron frastødning: Iltatomerne i hydroxylgrupperne har enlige elektronpar, der frastøder hinanden. Denne elektron-elektron frastødning destabiliserer yderligere den geminale diol.
3. Dannelse af et mere stabilt produkt: Dehydreringsreaktionen fører til dannelsen af en keton eller aldehyd, som er mere stabil end den geminale diol. Carbonylgruppen i ketoner og aldehyder stabiliseres ved resonans og er mindre elektronrig end hydroxylgrupperne i den geminale diol.
4. Ligevægtsskift: Dehydreringsreaktionen er en ligevægtsproces. Ligevægten begunstiger dog stærkt dannelsen af ketonen eller aldehydet på grund af deres større stabilitet.
5. Syrekatalyse: Dehydreringsreaktionen katalyseres ofte af syrer. Syrer protonerer hydroxylgrupperne, hvilket gør dem bedre til at forlade grupper. Dette letter fjernelse af vand og dannelsen af carbonylforbindelsen.
Mekanisme:
Dehydreringen af en geminal diol sker via en syrekatalyseret mekanisme.
1. Protonation: Syren protonerer en af hydroxylgrupperne, hvilket gør den til en bedre afgangsgruppe.
2. Tab af vand: Den protonerede hydroxylgruppe forlader som vand og danner en carbocation.
3. Deprotonering: En base (ofte vand) fjerner en proton fra et kulstof, der støder op til carbocationen, hvilket resulterer i dannelsen af en dobbeltbinding og en keton eller aldehyd.
Konklusion:
Ustabiliteten af geminale dioler skyldes primært sterisk hindring, elektron-elektron frastødning og dannelsen af et mere stabilt produkt. Dehydreringsreaktionen er en gunstig proces, der fører til dannelsen af ketoner eller aldehyder.
Sidste artikelpH 14:Forståelse af højalkaliske stoffer og eksempler
Næste artikelForståelse af hydrogenperoxid pH:Faktorer og overvejelser
 Varme artikler
Varme artikler
-
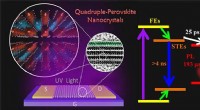 Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk
Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk -
 Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo
Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo -
 Lille volumen, høj-throughput organisk synteseByggestenstilgang til at forberede kompleks ─B(OH) 2 del indeholdende molekyler i stort antal. Kredit:Dömling Lab/Science Advances Universitetet i Groningen professor i lægemiddeldesign, Alexand
Lille volumen, høj-throughput organisk synteseByggestenstilgang til at forberede kompleks ─B(OH) 2 del indeholdende molekyler i stort antal. Kredit:Dömling Lab/Science Advances Universitetet i Groningen professor i lægemiddeldesign, Alexand -
 Nyt kulstof kan signalere trin-ændring for verdens mest populære batterierBatterier i elektriske køretøjer er en mulig applikation til OSPC-1. Kredit:Lancaster University Forskere har skabt en ny type kulstof, der kunne lave batterierne i vores telefoner, tablet compute
Nyt kulstof kan signalere trin-ændring for verdens mest populære batterierBatterier i elektriske køretøjer er en mulig applikation til OSPC-1. Kredit:Lancaster University Forskere har skabt en ny type kulstof, der kunne lave batterierne i vores telefoner, tablet compute
- Kan bævere rammes af kronisk svindsygdom?
- Elektrisk kabel udløser letvægts, opdagelse af brandsikker beklædning
- Hvad er strukturen af bregne?
- Skolen kan være skræmmende i en pandemi. En ny app hjælper lærere med at vide, hvordan børn har…
- Fremskridt medicin, lag for lag
- Tidevandsmose eller falsk habitat? Californiens miljøprojekt får kritik


