Molær koncentration ved STP:Forståelse af gasegenskaber
Her er hvorfor:
* Ideel gaslov: Den ideelle gaslov siger:PV =nRT, hvor:
* P =tryk
* V =volumen
* n =antal mol
* R =idealgaskonstant
*T =temperatur
* STP-betingelser: STP er defineret som 0°C (273,15 K) og 1 atm tryk.
* Molar koncentration: Molær koncentration (også kendt som molaritet) er antallet af mol af et stof pr. volumenenhed (mol/liter).
Afledning:
1. Fra den ideelle gaslov kan vi omarrangere for at få n/V =P/RT
2. Da n/V repræsenterer molær koncentration, kan vi se, at ved en given temperatur og tryk er den molære koncentration konstant uanset gassens identitet.
Derfor har alle ideelle gasser ved STP den samme molære koncentration, hvilket er ca. 0,0446 mol/L.
Vigtig bemærkning: Mens den molære koncentration er den samme for alle ideelle gasser ved STP, vil massefylden variere baseret på molekylvægten af hver gas. Dette skyldes, at en tungere gas vil have mere masse pr volumenhed, selvom antallet af mol pr volumenhed er det samme.
 Varme artikler
Varme artikler
-
 Følger kemikaliernes vej gennem jordenForskere fra Aarhus Universitet har udviklet en forbedret metode til at følge transporten af kemikalier gennem jorden. Kredit:Janne Hansen Hvor bliver pesticider og deres nedbrydningsprodukter a
Følger kemikaliernes vej gennem jordenForskere fra Aarhus Universitet har udviklet en forbedret metode til at følge transporten af kemikalier gennem jorden. Kredit:Janne Hansen Hvor bliver pesticider og deres nedbrydningsprodukter a -
 At lave biodiesel af beskidt gammel madolie er blevet meget nemmereSvampelignende katalysatorer kunne transformere biodieselproduktion og kemisk fremstilling. Billedet viser den porøse keramiske svamp fremstillet i undersøgelsen (forstørret 20, 000 gange). Kredit:RMI
At lave biodiesel af beskidt gammel madolie er blevet meget nemmereSvampelignende katalysatorer kunne transformere biodieselproduktion og kemisk fremstilling. Billedet viser den porøse keramiske svamp fremstillet i undersøgelsen (forstørret 20, 000 gange). Kredit:RMI -
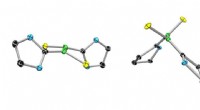 Generering af en stabil biradicalEn konventionel bor-bor dobbeltbinding (venstre) og dens ekstremt stabile biradiske slægtning. Kredit:Dr. Rian Dewhurst Bor har en række anvendelser, fra vaskeblegemiddel til varmebestandigt glas
Generering af en stabil biradicalEn konventionel bor-bor dobbeltbinding (venstre) og dens ekstremt stabile biradiske slægtning. Kredit:Dr. Rian Dewhurst Bor har en række anvendelser, fra vaskeblegemiddel til varmebestandigt glas -
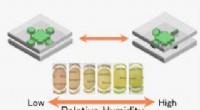 Funktionsfilm lavet af miljøvenlige lermineraler og farvestofferGennemsigtig hybridfilm sammensat af miljøvenlige lermineraler og farvestoffer, der ændrer farve med fugtighed via en ny mekanisme. Kredit:Shinsuke Takagi Forskere fra Tokyo Metropolitan Universit
Funktionsfilm lavet af miljøvenlige lermineraler og farvestofferGennemsigtig hybridfilm sammensat af miljøvenlige lermineraler og farvestoffer, der ændrer farve med fugtighed via en ny mekanisme. Kredit:Shinsuke Takagi Forskere fra Tokyo Metropolitan Universit
- Hvad er to eksempler på, hvordan densitet vil blive fysisk synlig i en blanding?
- Hvad er årsagen og virkningen af nummerstjerner?
- Hvilken type skyer ses i stormfulde dage?
- Hvad er virkningen af atomradius på den kemiske reaktivitet af halogenerne?
- Hvad er den primære energikilde?
- Opstod der sorte huller umiddelbart efter Big Bang?


