Forståelse af isomerer:Hvorfor forbindelser deler empiriske formler
Her er en oversigt:
* Empirisk formel: Viser det enkleste forhold mellem atomer i en forbindelse.
* Molekylformel: Viser det faktiske antal af hver type atom i et molekyle.
Eksempel:
* Glucose (C6H12O6) og eddikesyre (C2H4O2) begge har den samme empiriske formel:CH2O .
* Glucose har en molekylformel C6H12O6 , hvilket betyder, at den indeholder seks carbonatomer, tolv hydrogenatomer og seks oxygenatomer.
* eddikesyre har en molekylformel C2H4O2 , hvilket betyder, at den indeholder to carbonatomer, fire hydrogenatomer og to oxygenatomer.
Hvorfor sker det?
Kovalente forbindelser kan danne forskellige arrangementer af de samme atomer, hvilket resulterer i forskellige strukturer og egenskaber. Disse forskellige arrangementer kan føre til forskellige molekylære formler, men den samme empiriske formel.
Opsummering:
Den empiriske formel giver kun et forenklet billede af forbindelsens sammensætning. Den viser ikke det faktiske antal atomer i et molekyle, hvilket er nødvendigt for at skelne mellem forskellige kovalente forbindelser med samme empiriske formel.
 Varme artikler
Varme artikler
-
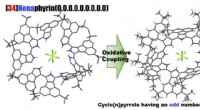 Syntese af en nær-infrarød lysabsorberende makrocyklisk aromatisk forbindelseSelektiv syntese af Cyclo [9] pyrroler Baseret på en oxidativ kobling. Kredit:Tetsuo Okujima, Ehime Universitet Profs. Okujima og Uno ved Ehime University, i samarbejde med prof. Kobayashi ved Shi
Syntese af en nær-infrarød lysabsorberende makrocyklisk aromatisk forbindelseSelektiv syntese af Cyclo [9] pyrroler Baseret på en oxidativ kobling. Kredit:Tetsuo Okujima, Ehime Universitet Profs. Okujima og Uno ved Ehime University, i samarbejde med prof. Kobayashi ved Shi -
 Forskere udvikler et effektivt system til levering af biomateriale til laboratorierKredit:National University of Science and Technology MISIS Materialeforskere fra NUST MISIS, sammen med kolleger fra Institut for Kemi ved Lomonosov Moscow State University, har udviklet en billig
Forskere udvikler et effektivt system til levering af biomateriale til laboratorierKredit:National University of Science and Technology MISIS Materialeforskere fra NUST MISIS, sammen med kolleger fra Institut for Kemi ved Lomonosov Moscow State University, har udviklet en billig -
 En robot og software gør det nemmere at skabe avancerede materialerEt team ledet af Rutgers tilpassede avanceret væskehåndteringsrobotik til at udføre den kemi, der kræves til at syntetisere syntetiske polymerer. Denne nye automatiserede tilgang muliggør hurtig udfor
En robot og software gør det nemmere at skabe avancerede materialerEt team ledet af Rutgers tilpassede avanceret væskehåndteringsrobotik til at udføre den kemi, der kræves til at syntetisere syntetiske polymerer. Denne nye automatiserede tilgang muliggør hurtig udfor -
 Farveskiftende bandager fornemmer og behandler bakterielle infektionerEn bandage ændrede farve fra grøn til gul, og fra grønt til rødt, i nærvær af stigende koncentrationer af lægemiddelfølsomme (DS) og lægemiddelresistente (DR) E coli , henholdsvis. Kredit:Tilpasset
Farveskiftende bandager fornemmer og behandler bakterielle infektionerEn bandage ændrede farve fra grøn til gul, og fra grønt til rødt, i nærvær af stigende koncentrationer af lægemiddelfølsomme (DS) og lægemiddelresistente (DR) E coli , henholdsvis. Kredit:Tilpasset


