Forståelse af kemiske buffere:Opretholdelse af pH-balance
Sådan fungerer de:
* Syrer frigiver hydrogenioner (H+) til en opløsning, hvilket gør den mere sur.
* Baser acceptere hydrogenioner (H+), hvilket gør en opløsning mindre sur (mere basisk eller basisk).
Buffere er opløsninger, der indeholder en svag syre og dens konjugerede base (eller en svag base og dens konjugerede syre). Disse komponenter kan reagere med tilsat syre eller base, hvilket minimerer ændringer i pH.
Her er nogle eksempler på buffersystemer:
* Bikarbonatbuffersystem: Dette system er afgørende for at opretholde blodets pH. Det involverer kulsyre (H2CO3) og dens konjugerede base, bicarbonat (HCO3-).
* Fosfatbuffersystem: Dette system er vigtigt i intracellulær væske. Det involverer dihydrogenphosphat (H2PO4-) og dets konjugerede base, hydrogenphosphat (HPO42-).
* Tris-buffer: Dette er en almindeligt anvendt laboratoriebuffer. Den består af Tris (tris(hydroxymethyl)aminomethan) og dens konjugerede syre, Tris-HCl.
Sådan fungerer buffere:
* Når en syre tilsættes: Bufferens konjugatbase reagerer med de tilsatte H+ ioner og omdanner dem til den svage syre. Dette minimerer ændringen i pH.
* Når en base tilføjes: Bufferens svage syre reagerer med de tilsatte OH-ioner og danner vand og konjugatbasen. Dette minimerer også ændringen i pH.
Opsummeret er buffere afgørende for at opretholde en stabil pH i biologiske systemer og forskellige kemiske reaktioner.
Sidste artikelSaltsyre- og aluminiumreaktion:afbalanceret ligning og forklaring
Næste artikelIlt- og klorbinding:Kovalent binding forklaret
 Varme artikler
Varme artikler
-
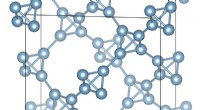 Ultralet aluminium:Kemikere rapporterer gennembrud inden for materialedesignSkematisk afbildning af en supertetrahedral aluminiumkrystalstruktur. Forskere fra Utah State University, USA og Southern Federal University, Rusland, beregningsmæssigt designet en ny, metastabil, ult
Ultralet aluminium:Kemikere rapporterer gennembrud inden for materialedesignSkematisk afbildning af en supertetrahedral aluminiumkrystalstruktur. Forskere fra Utah State University, USA og Southern Federal University, Rusland, beregningsmæssigt designet en ny, metastabil, ult -
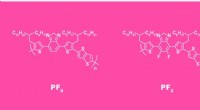 Forskere opgraderer organiske solceller til brug i tagsten, der producerer strømStrukturen af en gentagende enhed i polymerkæden uden fluor (venstre) og efter fluorering (højre). Kredit:Elena Khavina/MIPT Et internationalt team af materialeforskere fra Frankrig, Rusland og
Forskere opgraderer organiske solceller til brug i tagsten, der producerer strømStrukturen af en gentagende enhed i polymerkæden uden fluor (venstre) og efter fluorering (højre). Kredit:Elena Khavina/MIPT Et internationalt team af materialeforskere fra Frankrig, Rusland og -
 Tidlig in vitro -test for negative virkninger på embryonerEn chip med fire rækker af den nye embryotoksicitetstest. Kredit:ETH Zurich / Julia Boos ETH -forskere har kombineret embryonale celler og leverceller i en ny cellekulturtest. Denne kombination la
Tidlig in vitro -test for negative virkninger på embryonerEn chip med fire rækker af den nye embryotoksicitetstest. Kredit:ETH Zurich / Julia Boos ETH -forskere har kombineret embryonale celler og leverceller i en ny cellekulturtest. Denne kombination la -
 En ny guide til opdagelsesrejsende af den submikroskopiske verden inde i osDenne illustration skildrer arkitektur fundet i den submikroskopiske verden, som bestemt ved krystallografi. Kredit:Wladek Minor, UVA School of Medicine Forskere fra University of Virginia har eta
En ny guide til opdagelsesrejsende af den submikroskopiske verden inde i osDenne illustration skildrer arkitektur fundet i den submikroskopiske verden, som bestemt ved krystallografi. Kredit:Wladek Minor, UVA School of Medicine Forskere fra University of Virginia har eta
- Hvad er den mængde magt, der er nødvendig for at holde en bold i bevægelse, der er lanceret i fri…
- Hvordan orangutangmødre kommunikerer med deres afkom
- Amerikanske republikanere stemmer for at fjerne ulvebeskyttelsen
- Hvad er den kemiske formel for ammoniumchromat?
- Hvor oplades gaspartikler elektrisk?
- Hvad fik galakserne til at klynge efter Big Bang?


