Hydrogens neutrontal:Fra protium til tritium og deres praktiske anvendelser
TL;DR
De fleste brintatomer indeholder ingen neutroner. De sjældne isotoper deuterium og tritium indeholder henholdsvis en og to neutroner.
Baggrund
I løbet af det tidlige 20. århundrede var protonen og elektronen velkarakteriseret, men alligevel oversteg atommassetal konsekvent atomnumre, hvilket antydede, at en anden partikel med lignende masse - neutronen - var til stede i kernen. I 1932 bekræftede fysikeren James Chadwick dens eksistens.
Atomnummeret angiver antallet af protoner. Stabile, neutrale atomer har lige mange protoner og elektroner, hvilket giver dem en netto nulladning. Atommasseenheder (amu) er defineret som en tolvtedel af massen af et kulstof-12-atom, som indeholder 6 protoner og 6 neutroner; derfor en proton eller neutron ≈1amu.
Brintisotoper
Brint, det letteste grundstof, findes i tre stabile isotoper:
¹H – 0 neutrons (protium) ²H – 1 neutron (deuterium) ³H – 2 neutrons (tritium)
Alle isotoper bærer en enkelt proton og en enkelt elektron, der opretholder elektrisk neutralitet.
Applikationer
Protium (¹H)
Protium er den mest udbredte isotop. Mens frit brint sjældent findes på Jorden, danner det forbindelser som vand (H2O) og kulbrinter. Brintforbrænding udsender kun varme og vand, hvilket gør det til en ren energivektor.
Deuterium (²H)
Deuterium forekommer naturligt i et forhold på ~1 ud af 6.420 brintatomer. Når det parres med ilt, danner det tungt vand (D₂O), som har et højere frysepunkt (3,8°C) end almindeligt vand. Tungt vand tjener som neutronmoderator i atomreaktorer og er værdifuldt i videnskabelig forskning, selvom høje koncentrationer (>25%) kan være skadelige for biologiske væv.
Tritium (³H)
Tritium er radioaktivt, henfalder med en halveringstid på 12,28 år. Det produceres i atomreaktorer. På trods af sin radioaktivitet bruges tritium i langtidsholdbare lysende tegn, i sporingseksperimenter og i visse atomvåbendesigner.
 Varme artikler
Varme artikler
-
 Undersøgelse tilbyder ny indsigt i solopsamlingsteknologierCover af ACS Applied Energy Materials, der viser en katalysatormodificeret solcelle, der producerer brintbrændstof under forskellige lysforhold. Kredit:Grafisk af Jason Drees Hver time, solen mætt
Undersøgelse tilbyder ny indsigt i solopsamlingsteknologierCover af ACS Applied Energy Materials, der viser en katalysatormodificeret solcelle, der producerer brintbrændstof under forskellige lysforhold. Kredit:Grafisk af Jason Drees Hver time, solen mætt -
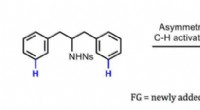 Kemikere opnår en vigtig milepæl for syntese:Fjern chiral induktionDen nye metode udviklet af Yu og kolleger. Kredit:Jin-Quan Yu/Scripps Research Kemikere ved Scripps Research har adresseret en af de mest formidable udfordringer inden for syntetisk kemi ved at
Kemikere opnår en vigtig milepæl for syntese:Fjern chiral induktionDen nye metode udviklet af Yu og kolleger. Kredit:Jin-Quan Yu/Scripps Research Kemikere ved Scripps Research har adresseret en af de mest formidable udfordringer inden for syntetisk kemi ved at -
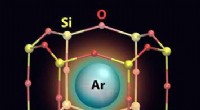 Studerer argongas fanget i todimensionel række små bureEn kunstnerisk gengivelse af et argon (Ar) atom fanget i et nanocage, der har en silicium (Si) -oxygen (O) ramme. Kredit:Brookhaven National Laboratory Forskere ved US Department of Energys (DOE)
Studerer argongas fanget i todimensionel række små bureEn kunstnerisk gengivelse af et argon (Ar) atom fanget i et nanocage, der har en silicium (Si) -oxygen (O) ramme. Kredit:Brookhaven National Laboratory Forskere ved US Department of Energys (DOE) -
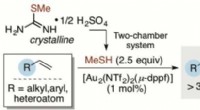 Forskere rapporterer om en enklere metode til sikker håndtering af methanthiol i kemisk synteseNy metode af professor Troels Skrydstrup ved Aarhus Universitet til hydrothiolering af π-systemer med overgangsmetalkomplekser. Kredit:Troels Skrydstrup Det kemiske grundstof svovl er en vigtig be
Forskere rapporterer om en enklere metode til sikker håndtering af methanthiol i kemisk synteseNy metode af professor Troels Skrydstrup ved Aarhus Universitet til hydrothiolering af π-systemer med overgangsmetalkomplekser. Kredit:Troels Skrydstrup Det kemiske grundstof svovl er en vigtig be


