Trin-for-trin guide til beregning af effektiv nuklear ladning
Af Rosann Kozlowski
6. juni 2023 kl. 23.44EST
AndreaObzerova/iStock/GettyImages
Effektiv nuklear ladning er den positive nettoladning, som et multielektronatoms valenselektroner oplever efter at have taget højde for den afskærmende effekt af indre elektroner. Over en periode stiger afgiften, mens den generelt falder ned ad en gruppe.
Effektiv nuklear ladningsformel
For en enkelt elektron udtrykkes forholdet som:
\(Z_{eff} =Z – S\)
- Z – atomnummeret (samlede protoner i kernen)
- S – afskærmningskonstanten, der repræsenterer den gennemsnitlige elektrontæthed, der reducerer den nukleare tiltrækning
- Zeff – den effektive kerneladning, som elektronen mærker
Beregning af effektiv nuklear ladning
Bestemmer Z og S kræver en klar forståelse af elektronkonfigurationen og anvendelsen af Slaters regler til at kvantificere afskærmning. Nedenfor er en praktisk, trin-for-trin procedure.
Trin 1:Identificer atomnummeret (Z)
Find grundstoffet på et periodisk system for at få dets atomnummer. For eksempel har natrium (Na) et atomnummer på 11.
Trin 2:Skriv elektronkonfigurationen
Udtryk konfigurationen ved hjælp af standardgrupperingssekvensen:\\((1s) (2s, 2p) (3s, 3p) (3d) (4s, 4p) (4d), (4f), (5s, 5p), (5d), (5f) …\\
For natrium:
\(\tekst{Na:} (1s^2)(2s^2,2p^6)(3s^1)\)
Her angiver overskriften antallet af elektroner i hver underskal. Valenselektronen af interesse er den enkelte 3s elektron.
Trin 3:Tildel afskærmningsværdier ved hjælp af Slaters regler
- Elektroner til højre for elektronen af interesse bidrager 0 til afskærmning.
- Elektroner i samme gruppe (samme hovedkvantetal og subshelltype) bidrager med 0,35 hver.
- For s- eller p-elektroner af interesse:
- Elektroner én skal under bidrager med 0,85 hver.
- Elektroner to eller flere skaller nedenfor bidrager med 1,00 hver.
- For d- eller f-elektroner af interesse bidrager alle andre elektroner med 1,00 hver.
Anvendelse af dette på natriums 3s elektron:
- Højre side:0
- Samme gruppe (ingen):0
- Skal 2 (8 elektroner):8 × 0,85 =6,80
- Skal 1 (2 elektroner):2 × 1,00 =2,00
- Shell 3 (ingen):0
Summen af afskærmningskonstanter:8,80 .
Trin 4:Beregn Zeff
Indsæt værdierne i formlen:
\(Z_{eff} =11 – 8,80 =2,20\)
Den effektive kerneladning, der virker på natriums valenselektron, er således 2,20. Denne værdi kan bruges til at forudsige ioniseringsenergier, atomare radier og andre elektroniske egenskaber.
Anvendelse af metoden på andre elementer
Den samme procedure fungerer for kationer, anioner og ethvert element, hvor elektronkonfigurationen er kendt. Nøjagtig registrering af antallet af protoner og elektroner sikrer et pålideligt skøn over den effektive nukleare ladning.
Sidste artikelEthanol vs. methanol:Hvilken brænder varmere?
Næste artikelForståelse af butanbrændstof:egenskaber, anvendelser og sikkerhed
 Varme artikler
Varme artikler
-
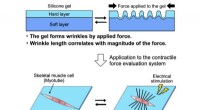 Forskere udvikler direkte mål for styrken af skeletmuskelmyotuberNår en kraft påføres et silikonegelsubstrat, opstår der rynker på overfladen. Det samme gælder, når et myotube på overfladen stimuleres med et elektrisk signal. Længden af rynkerne kan bruges til at
Forskere udvikler direkte mål for styrken af skeletmuskelmyotuberNår en kraft påføres et silikonegelsubstrat, opstår der rynker på overfladen. Det samme gælder, når et myotube på overfladen stimuleres med et elektrisk signal. Længden af rynkerne kan bruges til at -
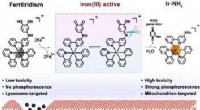 Siger mod mavekræft:Ny tilgang til selektiv kemoterapiKredit:Wiley Et nyt stof, kaldet FerriIridium, kan samtidigt hjælpe med at diagnosticere og behandle mavekræft. Den oprindeligt svagt aktive precursor (prodrug), baseret på en iridiumholdig forbi
Siger mod mavekræft:Ny tilgang til selektiv kemoterapiKredit:Wiley Et nyt stof, kaldet FerriIridium, kan samtidigt hjælpe med at diagnosticere og behandle mavekræft. Den oprindeligt svagt aktive precursor (prodrug), baseret på en iridiumholdig forbi -
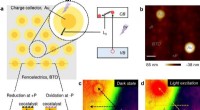 Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok,
Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok, -
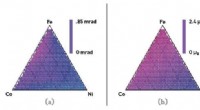 Kombineret datatilgang kan fremskynde udviklingen af nye materialerBilledtekst:(a) Kerr-rotationskortlægning af et jern, kobolt, nikkelkompositspredning ved hjælp af den mere nøjagtige højgennemstrømningsforsøgsmetode, (b) kun høj gennemløbsberegning, og (c) Iwasaki
Kombineret datatilgang kan fremskynde udviklingen af nye materialerBilledtekst:(a) Kerr-rotationskortlægning af et jern, kobolt, nikkelkompositspredning ved hjælp af den mere nøjagtige højgennemstrømningsforsøgsmetode, (b) kun høj gennemløbsberegning, og (c) Iwasaki


