Siger mod mavekræft:Ny tilgang til selektiv kemoterapi
Kredit:Wiley
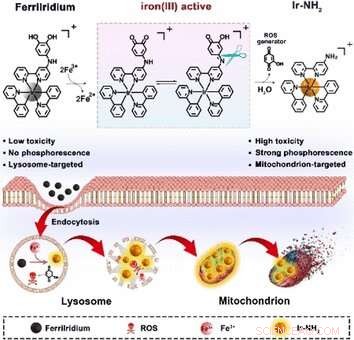
Et nyt stof, kaldet "FerriIridium, " kan samtidigt hjælpe med at diagnosticere og behandle mavekræft. Den oprindeligt svagt aktive precursor (prodrug), baseret på en iridiumholdig forbindelse, aktiveres først selektivt efter at have nået det indre af en tumorcelle. Dette er muligt på grund af den højere mængde jern, der er til stede der, rapporterer videnskabsmænd i tidsskriftet Angewandte Chemie . Selektiv aktivering reducerer uønskede bivirkninger.
Celler transporterer stoffer fra deres ydre til deres indre ved at folde sig ind i små områder af deres membran og derefter binde dem af (endocytose). Sådan kommer FerriIridium ind i målceller. De resulterende vesikler smelter derefter sammen med lysosomer. Disse celleorganeller har et surt miljø, der indeholder trivalente jernioner, Fe(III), og enzymer, hvormed de afmonterer cellekomponenter, der ikke længere er nødvendige. I mavekræftceller, Fe(III)-koncentrationen i lysosomerne er signifikant forhøjet.
Forskere, der arbejder med Yu Chen og Hui Chao ved Sun Yat-Sen University, Guangzhou, og Hunan University of Science and Technology, Xiangtan (Kina) gjorde brug af denne funktion. De udstyrede FerriIridium med en speciel funktionel gruppe (m-iminocatechol-gruppen), der selektivt binder til Fe(III). Når bundet, den funktionelle gruppe oxideres, mens jernionerne reduceres til Fe(II). Under de sure forhold i lysosomerne, FerriIridium opdeles derefter i to komponenter:et iridiumkompleks og et benzoquinonderivat.
Denne reaktionsmekanisme har en tredobbelt effekt. Først, Fe(II)-ioner kan katalysere en reaktion, der producerer meget reaktive hydroxylradikaler. Sekund, benzoquinoner er stærkt oxiderende. Med visse cellulære stoffer, såsom NADPH, de danner hydroxyquinoner, som reagerer med oxygen for at danne radikale oxygenarter, samt hydrogenperoxid, som igen kan reagere med Fe(II) og danne hydroxylradikaler. Benzoquinonforbindelser kan også forstyrre cellulær respiration. Radikalerne ødelægger lysosomerne, frigive deres indhold. Tredje, spaltningen af FerriIridium øger drastisk både phosphorescensen og toksiciteten af iridiumkomplekset. Fosforescensen kan bruges til at diagnosticere tumoren. Mest vigtigt, imidlertid, det giftige iridiumkompleks absorberes af mitokondrier, de "cellulære kraftværker." Det ødelægger dem indefra og ud ved at kollapse deres membranpotentiale. Sammen, disse virkninger fører til at mavekræftcellerne dør og tumorerne skrumper, som vist ved forsøg på cellelinjer og mus.
 Varme artikler
Varme artikler
-
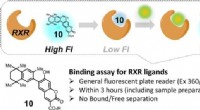 Syntetisk forbindelse giver hurtig screening for potentielle lægemidlerFluorescensen fra forbindelse 10 stiger, når en RXR-målretningsligand fortrænger den, hvilket gør det til en nyttig indikator for ligandaktivitet i assays. Kredit:Okayama University En simpel anal
Syntetisk forbindelse giver hurtig screening for potentielle lægemidlerFluorescensen fra forbindelse 10 stiger, når en RXR-målretningsligand fortrænger den, hvilket gør det til en nyttig indikator for ligandaktivitet i assays. Kredit:Okayama University En simpel anal -
 Nye alternativer kan lette efterspørgslen efter sjældne jordarters permanente magneterEnkeltkrystaller af CeCo 3 syntetiseret ved opløsningsvækstmetode. Kredit:Andriy Palaysuik Fra computerharddiske og smartphones til øretelefoner og elektriske motorer, magneter er på forkant med
Nye alternativer kan lette efterspørgslen efter sjældne jordarters permanente magneterEnkeltkrystaller af CeCo 3 syntetiseret ved opløsningsvækstmetode. Kredit:Andriy Palaysuik Fra computerharddiske og smartphones til øretelefoner og elektriske motorer, magneter er på forkant med -
 Nye bionedbrydelige polyurethanskum er udviklet af hvedestråKredit:CC0 Public Domain Hvert år produceres omkring 734 millioner tons hvedestrå på verdensplan, en stor mængde affald, som er billig og ikke har haft nogen veldefineret brug indtil nu. For nylig
Nye bionedbrydelige polyurethanskum er udviklet af hvedestråKredit:CC0 Public Domain Hvert år produceres omkring 734 millioner tons hvedestrå på verdensplan, en stor mængde affald, som er billig og ikke har haft nogen veldefineret brug indtil nu. For nylig -
 3-D printede væv og organer uden stilladsetKredit:CC0 Public Domain Konstrueret væv og organer er blevet dyrket med forskellige grader af succes i laboratorier i mange år. Mange af dem har brugt en stilladsfremgangsmåde, hvor celler sås på
3-D printede væv og organer uden stilladsetKredit:CC0 Public Domain Konstrueret væv og organer er blevet dyrket med forskellige grader af succes i laboratorier i mange år. Mange af dem har brugt en stilladsfremgangsmåde, hvor celler sås på
- Godt kolesterol nanopartikler søger og ødelægger kræftceller
- Hvad er EPA, og hvorfor er det i det varme sæde?
- Løst hud og slapt volumen beskytter Hagfish mod hajbid
- Afprøvning af et tilsluttet øko-kørselssystem i feltforsøg med tunge lastbiler
- Vi skal finde ud af, hvordan vi kan have sex i rummet for menneskelig overlevelse og velvære
- Holografisk stråleformning for at give et boost til metallisk 3-D-print


