Hvad sker der, når calcium møder 6M saltsyre? En omfattende guide
Af Emmalise Mac | Opdateret 30. august 2022
Når et stykke calciummetal indføres i en 6M saltsyreopløsning, sker der to forskellige, kraftige reaktioner. At forstå HCls grundlæggende syre-base-adfærd i vand er afgørende for at forudsige resultaterne, når Ca tilsættes.
Syredissociation i 6M HCl
Saltsyre er en stærk syre, der dissocierer fuldstændigt i vandig opløsning:
HCl-→H++Cl-
Protoner associeres med vand for at danne hydroniumioner:
H++H2O⇌H3O⁺
I en 6M opløsning er koncentrationen af H3O+ høj, hvilket giver en meget lav pH. Vandmolekyler forbliver til stede, hvilket tillader yderligere reaktioner.
Calciums reaktion med H₃O⁺ og H₂O
Calciummetal reagerer med hydroniumioner og vand og producerer calciumhydroxid og brintgas:
Ca+2H₃O⁺→Ca(OH)₂+H₂↑
Denne eksoterme proces frigiver varme og synlige brintbobler. Det friskdannede Ca(OH)2 dækker overfladen af opløsningen som et hvidt bundfald.
Danning af calciumchlorid
Samtidigt kombineres calciumioner med chloridioner og danner calciumchlorid, et opløseligt salt:
Ca2++2Cl-→CaCl2 (vandig)
CaCl2 forbliver opløst i opløsningen; der forekommer ingen synlig nedbør.
Disse reaktioner forskyder kollektivt ligevægten, reducerer hydroniumkoncentrationen og hæver beskedent pH, hvilket kan bekræftes af lakmuspapir.
 Varme artikler
Varme artikler
-
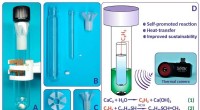 Kemikere opfinder et effektivt termisk kamera for at reducere omkostningerne til kemisk forskningReaktionsopsætningen ved hjælp af den udviklede rør-i-rør-reaktor:(A)—reaktoren klar til brug; (B)—den adskilte reaktor; (C)-nylonforing; (D)—termisk kamera og skemaet for rør-i-rør-reaktor og to trin
Kemikere opfinder et effektivt termisk kamera for at reducere omkostningerne til kemisk forskningReaktionsopsætningen ved hjælp af den udviklede rør-i-rør-reaktor:(A)—reaktoren klar til brug; (B)—den adskilte reaktor; (C)-nylonforing; (D)—termisk kamera og skemaet for rør-i-rør-reaktor og to trin -
 At skinne lys på en væske ændrer fuldstændig dens dielektriske permittivitetBlinkende blåt lys (venstre) på væsken fik den til at skifte til en høj dielektrisk permittivitetsfase, mens skinnende grønt lys på den (højre) vendte ændringen. Kredit:H. Nishikawa et al , CC BY 4.0
At skinne lys på en væske ændrer fuldstændig dens dielektriske permittivitetBlinkende blåt lys (venstre) på væsken fik den til at skifte til en høj dielektrisk permittivitetsfase, mens skinnende grønt lys på den (højre) vendte ændringen. Kredit:H. Nishikawa et al , CC BY 4.0 -
 LSU Chemical Engineering afslører nye destillationskolonnerJohn Pendergast, professional-in-residence i Cain Department of Chemical Engineering, og John Flake, formand for Cain Department of Chemical Engineering. Kredit:LSU College of Engineering LSU Cain
LSU Chemical Engineering afslører nye destillationskolonnerJohn Pendergast, professional-in-residence i Cain Department of Chemical Engineering, og John Flake, formand for Cain Department of Chemical Engineering. Kredit:LSU College of Engineering LSU Cain -
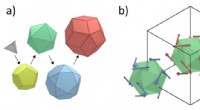 Kvasikrystalklar:Materiale afslører en unik forskydende overfladestruktur under mikroskopTsai-typen klynger sig inde i den anden af Au-Al-Tb tilnærmelsesvis videnskabsmændene valgte (a), og den tilsvarende spin -icosahedra (b). Kredit:Ryuji Tamura fra Tokyo University of Science Mel
Kvasikrystalklar:Materiale afslører en unik forskydende overfladestruktur under mikroskopTsai-typen klynger sig inde i den anden af Au-Al-Tb tilnærmelsesvis videnskabsmændene valgte (a), og den tilsvarende spin -icosahedra (b). Kredit:Ryuji Tamura fra Tokyo University of Science Mel
- Hvilken type apparat ville overføre elektrisk energi til sund energi?
- Hvilken procentdel af brint i peroxid?
- Hvad har al celle til fælles?
- Ceres er sandsynligvis dannet længere ude i solsystemet og migreret indad
- Ny elektronisk hud til proteser, robotteknologi registrerer tryk fra forskellige retninger
- Hvordan konverterer du magnetisk energi til lysenergi?


