Protoner vs. elektroner:Hvordan de former materiens byggesten
Af Lesley Barker – Opdateret Aug302022
Oversigt over atomstruktur
Atomer er de grundlæggende enheder af stof, hver unikt defineret af dens elektron-, proton- og neutronkonfiguration. Denne struktur bestemmer et elements identitet.
Elektroner:Den negative sky
Elektroner er praktisk talt masseløse, negativt ladede partikler, der kredser om kernen i diskrete energiskaller. Den maksimale belægning af hver skal følger 2n²-reglen, og den rumlige fordeling beskrives ofte som en elektronsky eller bølgefunktion.
Protoner:Positiv kerne
Protoner, der befinder sig i kernen, bærer en positiv ladning, der er lig med en elektrons. Deres tiltrækning af elektroner opretholder ladningsneutralitet i neutrale atomer. Antallet af protoner – atomnummeret – identificerer entydigt et grundstof.
Neutroner:Nuklear lim
Neutroner, der også er placeret i kernen, har ingen nettoladning, men giver den stærke kernekraft, der binder protoner sammen. Som Anthony Carpi fra City University of New York forklarer, virker neutroner som "lim", og forhindrer de frastødende kræfter mellem positivt ladede protoner i at destabilisere kernen.
Opladningsbalance og ioner
I et neutralt atom er antallet af protoner og elektroner identiske. Når denne balance er forstyrret, kaldes de resulterende ladede arter ioner, ikke atomer.
Atomtal og masse
Atomnummeret (Z) tæller protoner, og i et neutralt atom også elektroner. Atomvægt (eller massetal) tilnærmer summen af protoner og neutroner og kan findes i grundstoffernes periodiske system.
Ekspertindsigt
Både elektroner og protoner er ladede subatomære partikler; deres ladningstegn er forskellige, og elektroner er effektivt vægtløse, mens protoner har målbar masse. Elektroner kredser om kernen, tiltrukket af protonernes positive ladning.
Historiske milepæle:J.J. Thomson modtog Nobelprisen i 1906 for at opdage elektronen, og Ernest Rutherford identificerede protonen i 1918.
For yderligere læsning, se Periodic Table of Elements .
 Varme artikler
Varme artikler
-
 3-D-printharpikser i tandudstyr kan være giftige for reproduktiv sundhedKredit:CC0 Public Domain To kommercielt tilgængelige 3-D-printbare harpikser, som markedsføres som værende biokompatible til brug i dentale applikationer, let udvaskes forbindelser i deres omgivel
3-D-printharpikser i tandudstyr kan være giftige for reproduktiv sundhedKredit:CC0 Public Domain To kommercielt tilgængelige 3-D-printbare harpikser, som markedsføres som værende biokompatible til brug i dentale applikationer, let udvaskes forbindelser i deres omgivel -
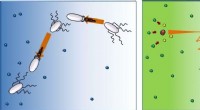 Enzymer og bakterier bevæger sig retningsbestemt, men bakterier mod mad, enzymer vækI nærværelse af mad (blå), bakterier (hvide) svømmer ligeud, skift derefter retning (tumle), og følg dette mønster igen og igen. Denne undersøgelse viser, at enzymer (røde) bevæger sig på samme måde,
Enzymer og bakterier bevæger sig retningsbestemt, men bakterier mod mad, enzymer vækI nærværelse af mad (blå), bakterier (hvide) svømmer ligeud, skift derefter retning (tumle), og følg dette mønster igen og igen. Denne undersøgelse viser, at enzymer (røde) bevæger sig på samme måde, -
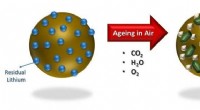 De ultimative betingelser for at få mest muligt ud af høj-nikkel-batterierVirkningerne af lagring af omgivende luft på overfladen af NMC-811 Kredit:WMG, University of Warwick Det er almindeligt kendt inden for batterifremstilling, at mange katodematerialer er fugtføls
De ultimative betingelser for at få mest muligt ud af høj-nikkel-batterierVirkningerne af lagring af omgivende luft på overfladen af NMC-811 Kredit:WMG, University of Warwick Det er almindeligt kendt inden for batterifremstilling, at mange katodematerialer er fugtføls -
 Photopower til mikrolabsKredit:Wiley-VCH Miniaturiserede enheder såsom mikrosensorer kræver ofte en uafhængig, lige så miniaturiseret strømforsyning. Søger efter passende systemer, Japanske videnskabsmænd har nu udviklet
Photopower til mikrolabsKredit:Wiley-VCH Miniaturiserede enheder såsom mikrosensorer kræver ofte en uafhængig, lige så miniaturiseret strømforsyning. Søger efter passende systemer, Japanske videnskabsmænd har nu udviklet
- Hvilket forekommer af to forskellige arter forsøger at besætte den samme niche?
- Hvordan man opbygger en Frog Trap
- Hvilken elektrolyt kan bruges til at elektrolysere vand?
- Hvad er den nærmeste stjerne på Jorden i de næste 10000 år?
- Hvad er det samlede reduktionspotentiale for en celle, hvor lithium (Li) reduceret og kviksølv (Hg)…
- ADP i biologi:Energivalutaen, der brænder liv


