Methanol vs. isopropylalkohol:Vigtigste forskelle forklaret
Af Eri Luxton | Opdateret 30. august 2022
Hvad er en alkohol?
I daglig tale refererer "alkohol" ofte til ethanol, den drikkelige forbindelse, der findes i drikkevarer. I kemi er en alkohol imidlertid enhver forbindelse, der indeholder en hydroxylgruppe (–OH) knyttet til et carbonatom [1] . Forståelse af denne definition tydeliggør, hvordan methanol og isopropylalkohol adskiller sig.
Methanol (CH3 ÅH)
Struktur:Et enkelt carbonatom bundet til tre hydrogenatomer og en hydroxylgruppe.
Nøgleegenskaber:
- Almindelig brug som et laboratorieopløsningsmiddel og som en komponent i denatureret alkohol.
- Indtagelse af selv en lille mængde kan føre til blindhed eller død – NIH Medline rapporterer [2] .
Isopropylalkohol (C3 H7 ÅH)
Struktur:Et centralt kulstof bundet til to methylgrupper og en hydroxylgruppe.
Nøgleegenskaber:
- Bedt brugt som opløsningsmiddel, desinfektionsmiddel og rengøringsmiddel.
- Mindre giftig end methanol, men stadig farlig ved indtagelse; det er meget brandfarligt.
Sikkerhedsadvarsel
Både methanol og isopropylalkohol er giftige, hvis de sluges, indåndes eller absorberes gennem huden. Brug dem altid i godt ventilerede områder, brug passende beskyttelsesudstyr, og hold dem utilgængeligt for børn og kæledyr.
 Varme artikler
Varme artikler
-
 Gelatine kan snart drive vores wearables og IoT-enhederFigur 1. Kæmpe termokraft af ioniske termoelektriske (i-TE) materialer. (A) i-TE materialer af gelatine- x KCl- m / n FeCN4-/3- ( x er KCl og m / n er K4Fe(CN)6/K3Fe(CN)6 molære koncentrat
Gelatine kan snart drive vores wearables og IoT-enhederFigur 1. Kæmpe termokraft af ioniske termoelektriske (i-TE) materialer. (A) i-TE materialer af gelatine- x KCl- m / n FeCN4-/3- ( x er KCl og m / n er K4Fe(CN)6/K3Fe(CN)6 molære koncentrat -
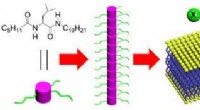 En ny metode til at transportere ioner gennem cellemembraner baseret på en enkelt aminosyreEkstremt simple monopeptider samler sig selv til stavlignende strukturer og videre til ringformede ensembler til mediering af højeffektiv transport af anioner i membranen. Kredit:Agency for Science, T
En ny metode til at transportere ioner gennem cellemembraner baseret på en enkelt aminosyreEkstremt simple monopeptider samler sig selv til stavlignende strukturer og videre til ringformede ensembler til mediering af højeffektiv transport af anioner i membranen. Kredit:Agency for Science, T -
 Nye elektronbriller skærper vores syn på atomare skala funktionerEn aberration-korrektionsalgoritme (nederst) gør atom probe tomografi (APT) på niveau med scanning transmission elektronmikroskopi (STEM) (øverst) - en industristandard - til karakterisering af urenhe
Nye elektronbriller skærper vores syn på atomare skala funktionerEn aberration-korrektionsalgoritme (nederst) gør atom probe tomografi (APT) på niveau med scanning transmission elektronmikroskopi (STEM) (øverst) - en industristandard - til karakterisering af urenhe -
 Forskere dechiffrere nøgleprincippet bag reaktion af metalloenzymerEntatilstandsmodelkomplekser optimerer energierne ved start og slutkonfiguration for at muliggøre hurtige reaktionshastigheder (illustreret af den kuperede jord). Arbejdet viser, at princippet om enta
Forskere dechiffrere nøgleprincippet bag reaktion af metalloenzymerEntatilstandsmodelkomplekser optimerer energierne ved start og slutkonfiguration for at muliggøre hurtige reaktionshastigheder (illustreret af den kuperede jord). Arbejdet viser, at princippet om enta
- Hvad er 158 kilo i sten og pund?
- Hvilken kombination af syre og base kan bruges til at fremstille saltkaliumchlorid KCI?
- Uddannelse er nøglen til lige forældrerettigheder for par af samme køn
- Hvad er den lille vinkelformel?
- Hvordan studerer videnskabsmand gammel atmosfære?
- Forståelse af pH Up:Almindelige baser og deres anvendelser


