Sådan skriver du en laboratorierapport om titrering:Trin-for-trin-vejledning
Af Veronica Mitchell | Opdateret 30. august 2022
Titreringer er en hjørnesten i analytisk kemi, der bruges til at bestemme den ukendte koncentration af et stof. Proceduren involverer omhyggelig, trin-for-trin tilsætning af en titrant til en opløsning, indtil reaktionen når fuldendelse, normalt signaleret ved en farveændring i en indikator. En burette registrerer den nøjagtige mængde titrant, der kræves, og dataene bruges derefter til at beregne analytkoncentrationen.
Trin 1:Bekræft overensstemmende resultater
Udfør titreringen mindst tre gange, og optag hver burettelæsning. Resultaterne er overensstemmende, hvis de ligger inden for 0,1 ml fra hinanden; kun overensstemmende data vil blive brugt i efterfølgende beregninger.
Trin 2:Udkast til introduktionen
Introducer formålet med eksperimentet, analytten af interesse og den anvendte reaktion. Inkluder den afbalancerede kemiske ligning, eksperimentelle forhold (pH, temperatur) og valget af indikator med en kort begrundelse for dens egnethed.
Trin 3:Detaljer om den eksperimentelle procedure
Beskriv, hvordan opløsningerne blev fremstillet, mængderne og koncentrationerne af reagenser og titreringsprotokollen. Bemærk eventuelle forholdsregler eller udførte kalibreringstrin.
Trin 4:Præsentér resultaterne
Tabulér dataene:endelig burettevolumen, initial burettevolumen og titeren (endelig-initial). Rapporter hver aflæsning med to decimaler (f.eks. 12,34 ml), og marker de overensstemmende værdier. Beregn middeltiteren fra det konkordante sæt og placer det under tabellen.
Trin 5:Udfør beregninger
Anvend det passende støkiometriske forhold ved hjælp af middeltiteren for at bestemme den ukendte koncentration. Vis hvert algebraisk trin, medtag enheder og afrund til to decimaler. Henvis om nødvendigt standardformler for volumetrisk analyse.
Trin 6:Skriv konklusionen
Opsummer den eksperimentelt afledte koncentration. Diskuter, om resultatet stemmer overens med forventede værdier, eventuelle fejlkilder og den overordnede pålidelighed af dataene.
Nødvendige materialer
- Fuldførte titreringsdata
- Pen og laboratorie-notesbog
- Videnskabelig lommeregner
 Varme artikler
Varme artikler
-
 Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj
Bifile overflader reducerer afrimningstider i varmevekslereTime-lapse billeder af dynamisk afrimning på superhydrofobe og bifile overflader. Tidspunktet t =0 repræsenterer det tidspunkt, hvor smeltning af frost først blev observeret visuelt. Kredit:Nenad Milj -
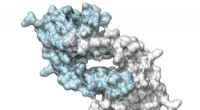 Designer enzym bruger unaturlig aminosyre til katalyseStruktur af LmrR, et protein med en stor pore ved dets dimere grænseflade, som kan binde antibiotika eller rekruttere substrater til at gennemgå katalyse. Kredit:Clemens Mayer / University of Groninge
Designer enzym bruger unaturlig aminosyre til katalyseStruktur af LmrR, et protein med en stor pore ved dets dimere grænseflade, som kan binde antibiotika eller rekruttere substrater til at gennemgå katalyse. Kredit:Clemens Mayer / University of Groninge -
 En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp
En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp -
 Hårde enkeltmolekylemagneter:Tetranukleære sjældne jordarters metalkomplekser med kæmpe spinKredit:Wiley Magneter dannet af et enkelt molekyle er af særlig interesse i datalagring, da evnen til at gemme lidt på hvert molekyle kunne øge computerens lagerkapacitet markant. Forskere har nu
Hårde enkeltmolekylemagneter:Tetranukleære sjældne jordarters metalkomplekser med kæmpe spinKredit:Wiley Magneter dannet af et enkelt molekyle er af særlig interesse i datalagring, da evnen til at gemme lidt på hvert molekyle kunne øge computerens lagerkapacitet markant. Forskere har nu
- Hvad er formlen for metallisk jern?
- Rapport giver vejledning i, hvordan man sikkert kan udforske store vandsystemer begravet under antar…
- Hvordan kan du fordoble accelerationen af et objekt, hvis ikke kan ændre masse?
- Hvad er definitionen af masse i biologi?
- Ny forskning for at afsløre, hvordan næringsstoffer driver giftige 'brunt tidevand' på østkysten…
- Kan latter helbrede sygdom?


