Illustration af et heliumatom:Trin-for-trin Bohr-modeltegning
Af Jack Brubaker
Opdateret 30. august 2022
Bohr-modellen – introduceret af fysiker Niels Bohr i 1913 – tilbyder en klar, visuel måde at introducere atomstruktur på. Det skildrer atomer som miniature solsystemer, med elektroner, der kredser om en tæt kerne. Selvom moderne kvantemekanik giver et mere nuanceret billede, forbliver Bohr-modellen et værdifuldt undervisningsredskab, især for tidlige kemistuderende.
Et neutralt heliumatom (den enkleste ædelgas) indeholder to protoner, to neutroner og to elektroner. Den følgende guide viser, hvordan man skitserer dette atom ved hjælp af Bohr-rammen.
Trin 1
Tegn en cirkel på cirka 5 cm i diameter. Dette vil repræsentere kernen.
Trin 2
Tilføj to "+"-symboler inde i kernen for at angive de to positivt ladede protoner.
Trin 3
Placer derefter to små "0"-symboler inden for den samme cirkel for at angive de to uladede neutroner.
Trin 4
Omslut kernen med en større cirkel, så der efterlades ca. en halv tomme (1,3 cm) mellemrum mellem de to cirkler. Denne ydre ring repræsenterer elektronbanen. Marker to små "e"-symboler på banen for at vise de to elektroner, der kredser om kernen.
TL;DR (for lang; læste ikke)
I et neutralt atom som helium er antallet af elektroner altid lig med antallet af protoner.
 Varme artikler
Varme artikler
-
 Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl
Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl -
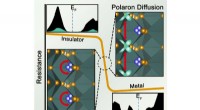 Team kaster nyt lys over design af uorganiske materialer til hjernelignende databehandlingFigur, der viser kobberionbevægelsen inden for et stift gitter af vanadium og ilt som kæden af en elektrisk ledningsevneændring i det kamæleonlignende materiale, der kan udnyttes til at skabe elektr
Team kaster nyt lys over design af uorganiske materialer til hjernelignende databehandlingFigur, der viser kobberionbevægelsen inden for et stift gitter af vanadium og ilt som kæden af en elektrisk ledningsevneændring i det kamæleonlignende materiale, der kan udnyttes til at skabe elektr -
 En ny metode til uafbrudt overvågning af faststofformalereaktionerDr. Stipe Lukin, Ruđer Bošković Instituttet. Kredit:Ruđer Bošković Institute Et hold af kemikere fra det kroatiske Ruđer Bošković Institut (RBI) beskrev en ny, letanvendelig metode til uafbrudt ov
En ny metode til uafbrudt overvågning af faststofformalereaktionerDr. Stipe Lukin, Ruđer Bošković Instituttet. Kredit:Ruđer Bošković Institute Et hold af kemikere fra det kroatiske Ruđer Bošković Institut (RBI) beskrev en ny, letanvendelig metode til uafbrudt ov -
 Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
- Savannabrande pumper centralafrikanske skove fulde af nitrogen
- Skal reelle overskud i virtuelle verdener beskattes? ISU-professorer siger, at der er en måde at gø…
- En ny algoritme muliggør mere realistiske lydeffekter i VR
- Termisk ledningsevne af metaller:Forståelse af videnskaben
- NASA satellit analyserer ny tropisk cyklon i det sydlige Stillehav
- Hvem etablerede det videnskabelige grundlag for vaccination?


