Forståelse af pH:Skalaen for surhed og alkalinitet i kemi
Af Robert Boumis – Opdateret 30. august 2022
pH-skalaen kvantificerer, hvor surt eller basisk et stof er, et hjørnestensbegreb inden for kemi, biologi, geologi og mange anvendte videnskaber. Beherskelse af pH gør det muligt for forskere at kommunikere kritiske egenskaber ved materialer med præcision.
Hvad er pH?
pH, altid skrevet med små bogstaver, måler koncentrationen af hydrogenioner (H⁺) i en opløsning. Skalaen går fra 0 til 14, hvor 7 repræsenterer neutralt rent vand. Værdier under 7 angiver stigende surhedsgrad, mens værdier over 7 indikerer stigende alkalinitet. Ekstremt sure eller basiske opløsninger kan være ætsende.
Skalaen er logaritmisk, hvilket betyder, at hver enhedsændring svarer til en ti gange forskel i hydrogenionkoncentration. For eksempel indeholder en opløsning med en pH-værdi på 4 ti gange mere H⁺ end en opløsning med en pH-værdi på 5.
Beregning af pH
Matematisk er pH defineret som den negative base-10 logaritme af hydrogenionkoncentrationen (udtrykt i mol pr. liter eller molaritet):
pH =–log10[H+]
Denne konvertering forenkler repræsentationen af hydrogenionniveauer, hvilket gør det nemmere at sammenligne løsninger.
Praktisk eksempel
Antag, at du har 1L af en opløsning, der indeholder 0,02 g brint. Da et mol hydrogen er ca. 1 g, er molariteten 0,02 molL⁻1 (eller 2×10⁻²M). At tage den negative log giver:
pH =–log₁₀(2×10⁻²) ≈ 1,7 (afrundet til 2 for nemheds skyld). Således er opløsningen stærkt sur.
Bestemmelse af pH ud fra pOH
pOH, den negative log for hydroxidionkoncentration, giver en indirekte vej til pH:
pOH =-log10[OH-]
Fordi [H⁺][OH⁻] =1×10⁻¹⁴ ved 25°C, er pH og pOH relateret af:
pH + pOH =14 → pH =14 – pOH
For eksempel giver en pOH på 12 en pH på 2. Den omvendte beregning bruger 14 – pH =pOH.
 Varme artikler
Varme artikler
-
 Video:Hvorfor lugter mine hundepoter som Fritos?Kredit:The American Chemical Society Mange mennesker synes at tro, at deres hvalps poter lugter af majsflis. Denne uge om reaktioner, vi tackler kemien bag den lugt, og bede folk snuse deres søde
Video:Hvorfor lugter mine hundepoter som Fritos?Kredit:The American Chemical Society Mange mennesker synes at tro, at deres hvalps poter lugter af majsflis. Denne uge om reaktioner, vi tackler kemien bag den lugt, og bede folk snuse deres søde -
 Nyligt syntetiseret svampemasse kan tænde en selvdestruerende knap for kræftKredit:Pixabay/CC0 Public Domain Kræftceller bruger en særlig teknik til at formere sig:De sletter deres programmerede død -gen gennem mutation, og tilsyneladende glemmer at dø, når deres levetid
Nyligt syntetiseret svampemasse kan tænde en selvdestruerende knap for kræftKredit:Pixabay/CC0 Public Domain Kræftceller bruger en særlig teknik til at formere sig:De sletter deres programmerede død -gen gennem mutation, og tilsyneladende glemmer at dø, når deres levetid -
 Forskere afslører in situ manipulation af aktivt guld-titandioxid-interfaceGeometrisk og elektronisk struktur af Au-TiO 2 grænseflade under CO/O 2 (EN, C, E) og O 2 miljø (B, D, F). Kredit:GAO Yi Et internationalt fælles forskerhold fra Shanghai Advanced Research I
Forskere afslører in situ manipulation af aktivt guld-titandioxid-interfaceGeometrisk og elektronisk struktur af Au-TiO 2 grænseflade under CO/O 2 (EN, C, E) og O 2 miljø (B, D, F). Kredit:GAO Yi Et internationalt fælles forskerhold fra Shanghai Advanced Research I -
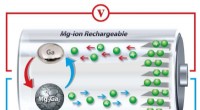 Selvhelbredende væske bringer nyt liv til batterialternativetI forskernes nye anodedesign, gallium smelter og størkner gentagne gange, helbredelse af de revner, der ellers gradvist ville mindske batteriets evne til at holde en opladning. Kredit:University of Pe
Selvhelbredende væske bringer nyt liv til batterialternativetI forskernes nye anodedesign, gallium smelter og størkner gentagne gange, helbredelse af de revner, der ellers gradvist ville mindske batteriets evne til at holde en opladning. Kredit:University of Pe
- Hvad kaldes lave flade områder af jord?
- Næsten 500 mennesker i det sydøstlige USA melder om meteor
- Ren luft er en homogen blanding?
- Team designer todimensionel radarreflektor til at måle subtile jordbevægelser
- Når Kinas forsknings- og udviklingsfinansiering ud til de rigtige virksomheder?
- Forskere udvikler nyt værktøj til analyse af store superledende kredsløb


