Selvhelbredende væske bringer nyt liv til batterialternativet
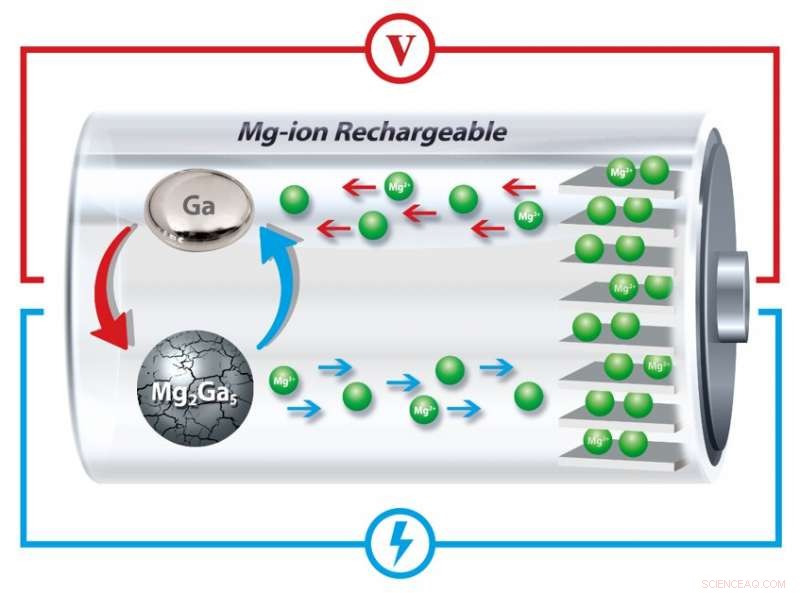
I forskernes nye anodedesign, gallium smelter og størkner gentagne gange, "helbredelse" af de revner, der ellers gradvist ville mindske batteriets evne til at holde en opladning. Kredit:University of Pennsylvania
Genopladelige lithium-ion (Li-ion) batterier er en revolutionerende teknologi, findes i alt fra mobiltelefoner til biler. Deres allestedsnærværende og rolle i at bryde afhængigheden af fossile brændstoffer gav en trio af forskere dette års Nobelpris i kemi.
Men selv om Li-ion batteriteknologi er ved at blive anerkendt med en af videnskabens toppriser, kemien bag dem står over for en truende udfordring. Lithium-ion-batterier kan ikke genoplades i det uendelige; materialerne i disse batteriers elektroder udvider sig og revner med hver cyklus, gradvist mindske deres opbevaringsydelse, indtil de er ubrugelige. Den resulterende efterspørgsel efter frisk lithium, kobolt og andre nødvendige elementer belaster naturressourcerne.
Med denne udfordring i tankerne, Penn Engineers søger at designe genopladelige batterielektroder, der kan arbejde effektivt med andre metalioner end lithium. Magnesium-ion-batterier er et lovende alternativ, men materialer, der reversibelt kan opbevare magnesium, har hidtil været endnu mere modtagelige for revner og andre problemer end deres Li-ion-fætre.
Penn-forskerne har nu fundet en løsning ved at inkorporere gallium, et metal, der har et smeltepunkt et par grader højere end stuetemperatur, ind i anoden på et magnesium-ion batteri. Ved at smelte og størkne med hver opladnings- og afladningscyklus, disse anoder kan "helbrede" revnedannelsen og den efterfølgende ekspansion, som normalt nedbryder genopladeligt batterilager.
Deres eksperimenter viser, at denne nye anode forlænger levetiden for magnesium-ion-batterier betydeligt, og gør det uden behov for dyre materialer i nanoskala. Disse egenskaber kan gøre magnesium-ion-batterier til en god egnethed til store applikationer, tage presset af lithiumressourcerne.
Forskerne demonstrerede deres gallium-baserede anode i en undersøgelse offentliggjort i Avancerede energimaterialer .
Undersøgelsen blev ledet af Eric Detsi, Stephenson Term Assistant Professor i Institut for Materialevidenskab og Engineering, sammen med Lin Wang og Samuel Welborn, kandidatstuderende i sit laboratorium. De samarbejdede med Vivek Shenoy, Eduardo D. Glandt Præsidentens fornemme professor ved Institut for Materialevidenskab og Teknik.
"For de fleste elektriske køretøjer, vægten af batteriet repræsenterer omkring en femtedel af køretøjets samlede vægt. At stole udelukkende på lithium-ion-batterier til at drive disse køretøjer rundt om i verden vil lægge en betydelig belastning på lithium- og koboltressourcer, der bruges i batterierne, " Detsi siger. "De bliver allerede dyrere på grund af efterspørgsel, og det globale koboltmarked er stærkt afhængigt af forsyninger fra lande med høje geopolitiske risici."
"Det er indlysende, at der er behov for alternative batteriteknologier, " siger han. "Ikke for at erstatte lithium, men for at understøtte lithium."
Opladning og afladning af et batteri involverer kemiske reaktioner, der tillader ioner at bevæge sig fra den ene elektrode på batteriet til den anden, opnå eller frigive elektroner i processen. Imidlertid, alle med en aldrende mobiltelefon eller bærbar computer ved, at disse batterier mister deres evne til at holde en opladning over tid. En af hovedårsagerne til, at disse batterier fejler, er, at opladnings- og afladningscyklussen involverer en fysisk transformation af materialerne i elektroderne. Når ioner er inkorporeret i elektroden, disse materialer udvider sig, og når ionerne frigives fra elektroden, materialerne revner. Denne proces fortsætter, indtil materialerne går i stykker og fysisk mister elektrisk kontakt med elektroderne, gør batteriet ubrugeligt.
"Den volumenændring, der sker i de fleste elektrodematerialer på grund af inkorporering og frigivelse af ioner, fører til revner og pulverisering. Det er en af de ting, der dræber et batteri, " siger Wang. "Denne pulverisering er forbundet med den stressopbygning, der kommer med en fast-fastfase-transformation."
"I vores nye arbejde, imidlertid, " siger Welborn, "i stedet for en transformation fra en type fast stof til en anden, det oprindelige faste materiale omdannes til en væske. Dette hæmmer revnedannelsen og pulveriseringen, fordi spændingerne forbundet med den normale faststof-faststof-transformation ikke længere er til stede."
Ved stuetemperatur, rent gallium er en formbar, sølvfarvet metal, der nemt kan forveksles med aluminium eller nikkel. Holder nogle i hånden, imidlertid, afslører hurtigt en unik egenskab:med et smeltepunkt på 85 grader Fahrenheit, kropstemperatur er nok til at forvandle et fast stykke gallium til en kviksølvlignende væske.
I forskernes nye undersøgelse, galliumet starter i en fast form, fordi det er legeret med magnesium i partikler af mikronstørrelse.
"For elektronisk at forbinde disse små stykker, "Wang siger, "vi sætter dem ind i et ledende netværk af kulfiber, kønrøg og grafen, som alle er bundet sammen med et bindemiddel."
Når magnesiumionerne skilles fra gallium, det omdannes til sin flydende tilstand, fordi batteriet fungerer ved temperaturer lidt over galliums smeltepunkt.
"Da det er samlet i dette netværk af andre materialer, " siger Welborn, "når gallium går fra fast til flydende, den bevæger sig ikke rundt, som du måske forventer, at en væske gør."
Ved at bruge røntgenstråler til at undersøge krystalstrukturen af materialerne inde i batteriet, forskerne viste, at når batteriet oplades, ioner vender tilbage til anoden og gendannes faste gallium-magnesium-partikler.
Kritisk, da disse partikler rekonstitueres med hver cyklus, de oplever ikke den slags revner, der i sidste ende nedbryder andre batterier.
Forskernes eksperimentelle batteri modstod mere end tusinde opladningscyklusser, cirka fem gange mere end det nuværende avancerede magnesium-ion-batteri.
"De tusinde cyklusser, der er demonstreret i dette arbejde, repræsenterer en væsentlig forbedring, Detsi siger, "men vores drøm er at drage fordel af denne unikke selvhelbredende adfærd til at designe et batteri, der kan oplades og aflades for evigt."
Grænsen på det nye batteris tusinde cyklus levetid skyldes ikke elektroden, men snarere elektrolytten, det flydende medium, der flytter ioner fra en elektrode til en anden. Tidligere forskning fra Detsis gruppe har vist, hvilken rolle elektrolytten spiller ved langsomt at nedbryde batterielektroderne, og det fremtidige arbejde vil fokusere på, hvordan man kan forbedre denne proces.
Heldigvis, som med designet af undersøgelsens selvhelbredende elektroder, arbejdet med dette aspekt af batteridesign involverer smarte anvendelser af kemi, snarere end omkostningskrævende nanoteknologiske teknikker medfører andre forsøg på at forlænge batteriets levetid.
"For at løse problemerne med lithium-ion-batterier, batterisamfundet bruger almindeligvis nanomaterialer, " siger Detsi. "Men syntesen af nanomaterialer kan være kompleks, hvilket betyder, at det kan være meget dyrt at fremstille tonsvis af nanomaterialer i industriel skala til batterianvendelser. En bemærkelsesværdig ting med vores design er, at der ikke er behov for at bruge nanomaterialer, hvilket gør denne klasse af batterier meget attraktive til store applikationer."
 Varme artikler
Varme artikler
-
 En ny bioproces til at omdanne plantematerialer til værdifulde kemikalierKredit:CC0 Public Domain Et team af forskere ved University of Illinois Urbana-Champaign udviklede en bioproces ved hjælp af manipuleret gær, der fuldstændigt og effektivt omdannede plantematerial
En ny bioproces til at omdanne plantematerialer til værdifulde kemikalierKredit:CC0 Public Domain Et team af forskere ved University of Illinois Urbana-Champaign udviklede en bioproces ved hjælp af manipuleret gær, der fuldstændigt og effektivt omdannede plantematerial -
 De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e
De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e -
 Forskere observerer direkte membranbindingen af α-synuclein i levende cellerForskere fra University of Konstanz og Free University of Amsterdam, i samarbejde med Bruker BioSpin udviklingsteamet, har for første gang haft held med den direkte spektroskopiske påvisning af bindin
Forskere observerer direkte membranbindingen af α-synuclein i levende cellerForskere fra University of Konstanz og Free University of Amsterdam, i samarbejde med Bruker BioSpin udviklingsteamet, har for første gang haft held med den direkte spektroskopiske påvisning af bindin -
 Seje flammer antændte i rummetVarme flammer (venstre) viger for kølige flammer (højre). Kredit:University of Maryland En opdagelse er blevet gjort i Jordens kredsløb - konstante sfæriske kølige diffusionsflammer. Målinger i di
Seje flammer antændte i rummetVarme flammer (venstre) viger for kølige flammer (højre). Kredit:University of Maryland En opdagelse er blevet gjort i Jordens kredsløb - konstante sfæriske kølige diffusionsflammer. Målinger i di


