Nanocontainere til målrettet lægemiddellevering
Kredit:RUDN Universitet
RUDN University bioingeniører har skabt magnetiske nanocontainere til smart levering af lægemidler til de ønskede organer eller væv, hvilket mindsker risikoen for bivirkninger. Et eksperiment på mus viste, at nanobeholderne er ugiftige. Resultaterne af undersøgelsen er offentliggjort i tidsskriftet Polymerer .
Farmaceutiske bivirkninger opstår ofte, fordi det aktive stof i lægemidlet trænger ind i sunde organer. Det er derfor, for eksempel, kemoterapi er så svært for patienter i behandlingen af kræft:Giftige lægemidler påvirker ikke kun tumorceller, men hele kroppen. Målrettede lægemiddelleveringssystemer løser dette problem. Mange potentielle bærere er blevet foreslået i de senere år:mikrokapsler med en skal af polyelektrolytter, kunstige liposomer af mikro- og nanoskala, og protein nanopartikler, for eksempel. Flere dusin lægemidler pakket i sådanne beholdere bruges allerede i praksis eller er under kliniske forsøg.
Imidlertid, der er stadig mange problemer, der forhindrer den udbredte brug af smarte transportører. Den ene er, at afhængigheden af lægemiddelbiodistributionsprocessen i væv dikterer størrelsen af beholdere. Jo mindre størrelse, jo større er sandsynligheden for, at lægemidlet når det rigtige organ, og jo lavere dosis af lægemidlet er påkrævet, reducerer toksiske virkninger. Et andet problem er manglen på information om toksicitet, effekter på kroppen og fordeling i levende væv. Begge disse problemer er blevet løst med succes af RUDN Universitetets biokemikere i samarbejde med kolleger fra Rusland og Storbritannien.
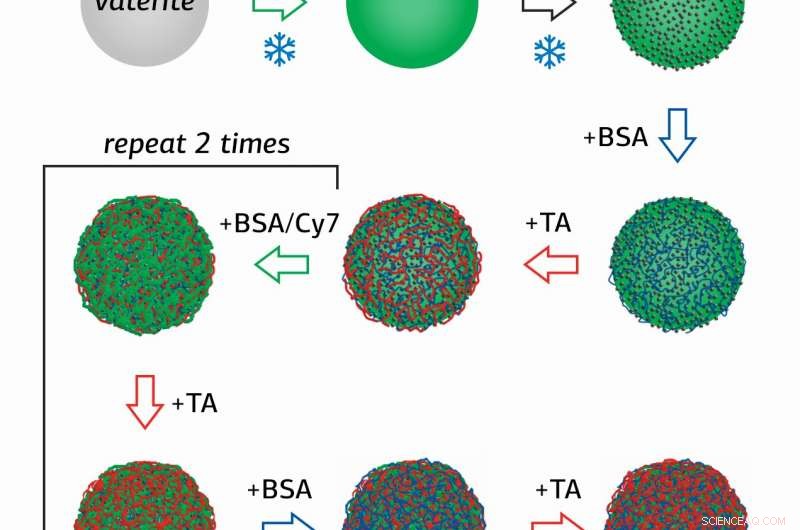
Forsker ved Surface Engineering Laboratory ved RUDN University Olga Sindeeva og hendes medforfattere skabte magnetisk følsomme beholdere i submikronskala - partikler på 400-600 nanometer, med en skal af flere lag bovint serumalbumin (BSA) med et fluorescerende tag Cy7, og garvesyre (TA).
Det nye ved undersøgelsen er metoden til at opnå beholdere, hvori nanopartikler af magnetit (MNP'er), blandet jernoxid (II, III) blev først adsorberet på overfladen af porøse granulat af calciumcarbonat, som derefter blev coatet sekventielt med flere lag af BSA-Cy7 og TA. Derefter, Calciumcarbonat blev vasket ud af beholderne under anvendelse af en vandig opløsning med et chelateringsmiddel.
"Med denne metode, det var muligt at fordoble mængden af magnetit i beholdere i forhold til, hvad man opnår ved adsorption og co-deposition metoder. Dermed, det er muligt at øge det magnetiske moment af nanobeholdere og øge hastigheden af deres bevægelse i det vaskulære system, Olga Sindeeva forklarede.
Bioingeniører fra RUDN Universitet forventer, at beholdernes submikronstørrelse øger biotilgængeligheden af det lægemiddel, der er indlæst i MNPs (BSA-Cy7-TA) beholderen.
Foreløbige forsøg på to cellelinjer, HeLa og fibroblaster, har vist, at beholderne ikke påvirker cellernes levedygtighed og kan anvendes in vivo.
De medicinfrie beholdere blev derefter testet på levende BALB/c-mus af begge køn, der vejede omkring 20 gram, 10 personer per gruppe. Beholdere i form af en suspension i saltvandsopløsning blev injiceret i halevenen på bedøvede mus. En suspension af magnetitfrie beholdere (BSA-Cy7-TA) blev anvendt som kontrol. Derefter, det ene af bagbenene på musene blev udsat for et magnetfelt i en time, mens det andet blev efterladt frit til sammenligning. Fordelingen af nanocontainere i væv fra levende mus blev observeret ved hjælp af magnetisk resonansbilleddannelse (MRI) og fluorescerende tomografi. Magnetometrisk analyse og histologisk undersøgelse af postmortem musevæv blev også udført en time efter fjernelse af magneten.
RUDN Universitetsbiologer har vist, at i de perifere kar af bagbenene i hvile ved en lav blodgennemstrømningshastighed, MNPs(BSA-Cy7-TA)-partikler bevæger sig i den første time efter intravenøs injektion i retning af det lem, som magneten er fastgjort til.
MR viste, at koncentrationen af magnetit i musklen nær magneten passerer gennem maksimum. Magnetitmængden viste sig at være 70 procent højere end i det frie lem. Derefter, magnetitsignalet faldt til baggrundsværdier.
Ifølge resultaterne af histologiske undersøgelser og magnetometri, forskerne fandt ud af, at MNP'er (BSA-Cy7-TA) hovedsageligt koncentrerede sig i lungerne, og, i mindre grad, i lever og milt. I øvrigt, deres koncentration i lungerne var fire til fem gange højere. En lille mængde af bæreren blev også fundet i andre indre organer og muskler, men koncentrationen var signifikant lavere end i lungerne. Dermed, biokemikere konkluderede, at fordelingen af intravenøse beholdere afhænger af blodforsyningen til organerne, det er, på hastigheden af blodgennemstrømningen, men er følsom over for lokaliseringen af magnetfeltet.
Der blev lagt særlig vægt på toksiciteten af intravenøse beholdere og deres virkninger på kroppen. Foreløbige test har vist, at in vitro i plasma eller blod, en betydelig procentdel af containerne ødelægges i løbet af en dag. Resultaterne af undersøgelserne tyder på, at beholderne har tid til at nå målet med intravenøs injektion. Derefter, ved at ændre fluorescenssignalet, bærerpartiklerne nedbrydes gradvist og udskilles fra kroppen.
Partiklerne er ikke-toksiske og hæmokompatible, og deres størrelse gør det muligt for dem at trænge ind i kroppens væv, men i arbejdsdoser, de skader ikke åndedræts- eller kredsløbssystemet, og påvirker ikke nyre- eller leverfunktioner. Aktiveringen af komplementsystemet, der er nødvendig for bionedbrydning af proteinmembranen i beholderne, påvirker ikke niveauet af leukocytter, og fører derfor ikke til nogen mærkbar systematisk betændelse.
Dermed, RUDN Universitetets forskere var i stand til at konstruere og distribuere beholdere med en høj mængde magnetit i kroppen, og effektivt styre deres implementering ved hjælp af et magnetfelt.
I fremtiden, Projektdeltagerne har til hensigt at skabe smarte nanokapsler, der kan levere lægemidlet til det rigtige organ og åbne for at frigive det aktive stof. Denne metode til lægemiddellevering ville undgå bivirkninger af behandlingen. Patienter med en række sygdomme, herunder børn eller ældre mennesker med dårligt helbred, kunne behandles med lægemidler, som ellers kunne undgås på grund af bivirkninger, der forværrer patientens tilstand.
 Varme artikler
Varme artikler
-
 Skittles videnskabsprojektideerSkittles er mere end bare en lækker slik. Når det kommer til skoleprojekter, kan disse små, farverige godbidder tjene som grundlag for en lang række eksperimenter, som blænder både dine klassekamme
Skittles videnskabsprojektideerSkittles er mere end bare en lækker slik. Når det kommer til skoleprojekter, kan disse små, farverige godbidder tjene som grundlag for en lang række eksperimenter, som blænder både dine klassekamme -
 Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit
Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit -
 Sådan beregnes PH af pufferløsningerEn puffer er en vandig opløsning designet til at opretholde en konstant pH, selv når den udsættes for små mængder syrer eller baser. Uanset om det er surt (pH 7), består en pufferopløsning af en svag
Sådan beregnes PH af pufferløsningerEn puffer er en vandig opløsning designet til at opretholde en konstant pH, selv når den udsættes for små mængder syrer eller baser. Uanset om det er surt (pH 7), består en pufferopløsning af en svag -
 Cryo-EM-strukturer af nikotinreceptoren kan føre til nye terapier for afhængighedTredimensionelle strukturer af nikotinacetylcholinreceptor bestemt af cryo-EM, med tilladelse fra Hibbs Lab. Kredit:Hibbs Lab, UT Southwestern Medical Center UT Southwestern forskere offentliggjor
Cryo-EM-strukturer af nikotinreceptoren kan føre til nye terapier for afhængighedTredimensionelle strukturer af nikotinacetylcholinreceptor bestemt af cryo-EM, med tilladelse fra Hibbs Lab. Kredit:Hibbs Lab, UT Southwestern Medical Center UT Southwestern forskere offentliggjor
- Gamle samfund holder lektioner for moderne byer
- Undersøgelse:Øget varme-tørke kombinationer kan skade afgrøder globalt
- Sådan Leach Gold Ore Med Chlorination
- Med en blid berøring, forskere skubber os tættere på flashhukommelses efterfølger
- Grace opgraderet til orkan, tager til Mexico
- Typer af svampe i Tundra


