Mestring af skeletligninger:Trin-for-trin guide til afbalancering af kemiske reaktioner
Af Grant D. McKenzie • Opdateret 30. august 2022
Kemistuderende bruger rutinemæssigt skeletligninger som et grundlæggende værktøj til at afbalancere reaktioner. Reaktanterne er skrevet på venstre side, produkterne til højre, og en pil forbinder dem, hvilket giver ligningen dens "skelet"-struktur. At udfylde ligningen kræver at bestemme de korrekte støkiometriske koefficienter, som angiver de relative mængder af hver art.
Trin 1:List reaktanterne
Identificer alle reaktanter og placer dem på venstre side adskilt af plustegn. Følg reaktanterne med en reaktionspil. For eksempel, hvis calciumchlorid og natriumsulfat reagerer, skriv:
CaCl2 + Na2 SO4 →
Trin 2:Skriv produkterne
Placer de tilsvarende produkter på højre side af pilen, igen adskilt af plustegn. I eksemplet ovenfor er produkterne calciumsulfat og natriumchlorid:
CaCl2 + Na2 SO4 → CaSO4 + NaCl
På dette stadium er ligningen stadig et skelet, da antallet af natrium- og kloratomer ikke stemmer overens på begge sider.
Trin 3:Tilføj tilstandssymboler
Tilstandssymboler tydeliggør de fysiske forhold for hver forbindelse - fast (s), væske (l), gas (g) eller vandig opløsning (aq). I vores eksempel kombineres to vandige opløsninger for at danne en vandig opløsning og et fast bundfald:
CaCl2 (aq) + Na2 SO4 (aq) → CaSO4 (s) + NaCl (vandig)
Med tilstandssymbolerne på plads er skeletligningen klar til koefficientbalancering, hvilket sikrer massebevarelse på tværs af reaktionen.
Disse trin giver en klar ramme for at konstruere skeletligninger, før de anvender algebraiske metoder til at afbalancere dem.
Sidste artikelForståelse af rustdannelse:kemi, årsager og forebyggelse
Næste artikelForstå, hvordan man løser en blanding af forbindelser
 Varme artikler
Varme artikler
-
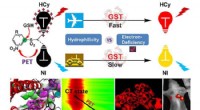 Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning
Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning -
 En dag til at fejre kemiens yndlingsenhed - muldvarpen. Men hvad er en muldvarp?Mole Day er en uofficiel helligdag, der fejres blandt kemikere den 23. oktober, mellem 6:02 og 18:02. Tid og dato er afledt af Avogadros nummer. Kredit:Ekaterina_Minaeva/Shutterstock.com Den 23. o
En dag til at fejre kemiens yndlingsenhed - muldvarpen. Men hvad er en muldvarp?Mole Day er en uofficiel helligdag, der fejres blandt kemikere den 23. oktober, mellem 6:02 og 18:02. Tid og dato er afledt af Avogadros nummer. Kredit:Ekaterina_Minaeva/Shutterstock.com Den 23. o -
 Hvorfor potentiometrisk titrering er afgørende for analyse med høj renhedAf Dianne Hermance Opdateret 24. marts 2022 Sinhyu/iStock/GettyImages I den farmaceutiske industri kan renheden af en forbindelse være forskellen mellem terapeutisk succes og fiasko. Potentiometris
Hvorfor potentiometrisk titrering er afgørende for analyse med høj renhedAf Dianne Hermance Opdateret 24. marts 2022 Sinhyu/iStock/GettyImages I den farmaceutiske industri kan renheden af en forbindelse være forskellen mellem terapeutisk succes og fiasko. Potentiometris -
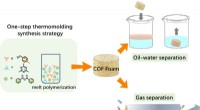 Ved brug af smeltepolymerisation til fremstilling af robuste kovalente organiske rammeskumKonstruer kovalente organiske rammer skumseparatorer ved smeltepolymerisation. Kredit:Science China Press Adsorptionsbaserede (f.eks. gas- eller væskemolekyler) separationsteknologier har vist unik
Ved brug af smeltepolymerisation til fremstilling af robuste kovalente organiske rammeskumKonstruer kovalente organiske rammer skumseparatorer ved smeltepolymerisation. Kredit:Science China Press Adsorptionsbaserede (f.eks. gas- eller væskemolekyler) separationsteknologier har vist unik
- Når en oceanisk plade skubbes under en kontinental, hvilket resulterer i vulkansk aktivitet, danner…
- Spor mængder isotop fra Fukushima -katastrofen fundet i Californiens vin
- En påstand om, at en maskine, der løber for evigt, derfor producerer så meget energi aa, den forb…
- Fortrænger mindre reaktive halogener flere?
- Hvilke parametre kræves for vækst af celler i dyrecellekultur?
- Tilstandsændring og kæmpe pulser fundet i en pulsar på millisekunder


