Beregning af den teoretiske koncentration af hydroniumioner (H₃O⁺)
Af Timothy Banas, Opdateret 30. august 2022
I rent vand gennemgår en lille del af molekylerne autoionisering, hvilket genererer hydronium- (H₃O⁺) og hydroxid- (OH⁻)-ioner. Koncentrationen af H₃O⁺ bestemmer en opløsnings surhedsgrad, kvantificeret ved dens pH. pH-skalaen går fra 0 (meget surt) til 14 (meget alkalisk), og det er et logaritmisk mål for hydroniumionkoncentrationen.
Trin 1:Bestem pH
Identificer opløsningens pH. For kendte reagenser er værdien normalt trykt på etiketten eller angivet i en referencetabel. Hvis pH-værdien er ukendt, skal du måle den med et kalibreret pH-meter eller udføre en titrering.
Trin 2:Omarranger pH-formlen
Forholdet mellem pH og hydroniumkoncentration er:
pH =–log₁₀[H₃O⁺]
Omarrangering giver:
[H₃O⁺] =10 –pH
Trin 3:Beregn koncentrationen
Indsæt den målte pH-værdi i ligningen. For eksempel giver en opløsning med pH=2:
[H₃O⁺] =10 –2 =1,0 x 10⁻²molL⁻¹
Opløsningen indeholder således 0,01 mol hydroniumioner pr. liter.
 Varme artikler
Varme artikler
-
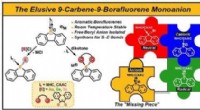 Stabilisering af borafluorenanionen med carbenerKredit:Wiley-VCH, Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202103628 Inkorporeringen af bor i polycykliske aromatiske kulbrintesystemer fører til interessante kromofore
Stabilisering af borafluorenanionen med carbenerKredit:Wiley-VCH, Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202103628 Inkorporeringen af bor i polycykliske aromatiske kulbrintesystemer fører til interessante kromofore -
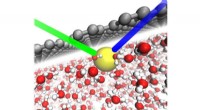 Den subtile rolle af overflader i ion-klæbrighedI vand (røde og hvide strukturer), den direkte interaktion mellem grafen (grå) og en thiocyanat (SCN‒) ion (gul) får ionen til at adsorbere til overfladen. De grønne og blå linjer repræsenterer indfal
Den subtile rolle af overflader i ion-klæbrighedI vand (røde og hvide strukturer), den direkte interaktion mellem grafen (grå) og en thiocyanat (SCN‒) ion (gul) får ionen til at adsorbere til overfladen. De grønne og blå linjer repræsenterer indfal -
 Kvantekemi løser mysteriet med de 20 aminosyrer i den genetiske kodeDe første 13 aminosyrer er karakteriseret ved meget ens kemisk hårdhed og elektroniske energiniveauer (vist på billedet som en enkelt cirkel). De nye aminosyrer blev mere og mere blødere og mere indiv
Kvantekemi løser mysteriet med de 20 aminosyrer i den genetiske kodeDe første 13 aminosyrer er karakteriseret ved meget ens kemisk hårdhed og elektroniske energiniveauer (vist på billedet som en enkelt cirkel). De nye aminosyrer blev mere og mere blødere og mere indiv -
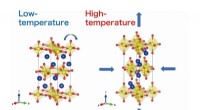 Undersøgelse undersøger bemærkelsesværdig negativ termisk ekspansion set i lagdelte ruthenaterDe strukturelle forvrængninger i Ca 2 RuO 4 er ansvarlige for dens anisotrope termiske ekspansion. Kredit:Masaki Azuma fra Tokyo Institute of Technology En tidligere ubemærket monoklinisk forv
Undersøgelse undersøger bemærkelsesværdig negativ termisk ekspansion set i lagdelte ruthenaterDe strukturelle forvrængninger i Ca 2 RuO 4 er ansvarlige for dens anisotrope termiske ekspansion. Kredit:Masaki Azuma fra Tokyo Institute of Technology En tidligere ubemærket monoklinisk forv
- Hvordan vil du vide, om et sammensat bundfald efter substitutionsreaktion?
- Vil Pebble smartwatch være i stand til at konkurrere med Apple og Google?
- Hvad er en videnskabsmand, der studerer bevægelse og kræfter?
- Tilskynder rabatter for kulstofpriser til en reduktion i emissioner?
- Hvilken kraft fungerer mod et objekt, der rejser vandret?
- Hvordan bliver forbliver forstenede fossiler?


