Beregning af teoretisk udbytte:en trin-for-trin guide i muldvarpe og gram
Af Emma Francesca • Opdateret 30. august 2022
I en kemisk reaktion kombineres reaktanter i præcise støkiometriske forhold for at danne produkter. Under ideelle laboratorieforhold kan du forudsige præcis, hvor meget produkt der vil komme ud af en given mængde reaktant. Den forudsagte mængde kaldes det teoretiske udbytte. At beregne det nøjagtigt kræver at kende mængden af reaktanter og produkter, der faktisk anvendes, og identificere den begrænsende reaktant.
Trin 1 – Skriv den balancerede ligning
Begynd med en korrekt afbalanceret kemisk ligning. Dette sikrer, at molforholdene mellem reaktanter og produkter er nøjagtige.
Trin 2 – Bestem molære masser
Brug et pålideligt periodisk system til at summere atomvægtene af alle atomer i hver art. Disse værdier er dine molære masser.
Trin 3 – Identificer støkiometriske forhold
Fra den afbalancerede ligning skal du notere molforholdene. For eksempel, hvis 1 mol af reaktant A producerer 2 mol af produkt B, er forholdet 1:2.
Trin 4 – Sammenlign faktiske beløb med ligningen
Hvis de mængder, du har, svarer til dem i den afbalancerede ligning, er det teoretiske udbytte lig med produktmængden vist i ligningen. Konverter denne værdi til gram ved at gange mol med produktets molære masse.
Trin 5 – Konverter gram til mol
Når du starter med masser i gram, skal du dividere hver med dens molære masse for at opnå mol.
Trin 6 – Identificer den begrænsende reaktant
Brug de støkiometriske forhold fra trin 3 til at sammenligne de mol, du har (fra trin 5) med de påkrævede mol. Den reaktant, der først løber ud, begrænser reaktionen.
Trin 7 – Beregn det teoretiske udbytte
Anvend molforholdet mellem den begrænsende reaktant og det ønskede produkt. For eksempel, hvis 2 mol af den begrænsende reaktant producerer 3 mol produkt, så giver 1 mol af den begrænsende reaktant 1,5 mol produkt.
Trin 8 – Konverter mol produkt til gram
Multiplicer de teoretiske mol produkt med dets molære masse for at opnå udbyttet i gram.
TL;DR (for lang; læste ikke)
Hvis en reaktion involverer en enkelt reaktant, er denne reaktant automatisk den begrænsende reaktant.
Referencer
- "Kemi" – John Olmsted et al., 2006
 Varme artikler
Varme artikler
-
 Mål havvands saltholdighed med tillid:En praktisk guideAf Susan Reynolds Opdateret 24. marts 2022 Saltvand, der indeholder havliv, skal indeholde en passende mængde saltvand - omkring 32 til 37 promille - for at opretholde sit økosystem. Saltniveauet k
Mål havvands saltholdighed med tillid:En praktisk guideAf Susan Reynolds Opdateret 24. marts 2022 Saltvand, der indeholder havliv, skal indeholde en passende mængde saltvand - omkring 32 til 37 promille - for at opretholde sit økosystem. Saltniveauet k -
 Mestring af Lewis Dot Structures:Sådan tælles valenselektroner for ethvert elementAf Sean Lancaster Opdateret 30. august 2022 Lewis-punktdiagrammer giver en kortfattet visuel repræsentation af valens-elektronfordeling i kovalente molekyler, hvilket giver kemikere mulighed for hur
Mestring af Lewis Dot Structures:Sådan tælles valenselektroner for ethvert elementAf Sean Lancaster Opdateret 30. august 2022 Lewis-punktdiagrammer giver en kortfattet visuel repræsentation af valens-elektronfordeling i kovalente molekyler, hvilket giver kemikere mulighed for hur -
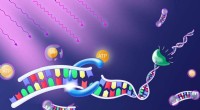 Programmering med lyskontaktenUdsættelse for lys frigiver molekylet ATP. Det giver energien til et enzym (blåt), der forbinder DNA-byggesten til en streng. Et andet enzym (grønt) adskiller strengen ved disse bindingssteder, sålede
Programmering med lyskontaktenUdsættelse for lys frigiver molekylet ATP. Det giver energien til et enzym (blåt), der forbinder DNA-byggesten til en streng. Et andet enzym (grønt) adskiller strengen ved disse bindingssteder, sålede -
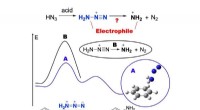 Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering
Kemikere beviser mekanismen for direkte aminering fra benzenDet grafiske abstrakt af direkte aminering. Kredit:Tomsk Polytechnic University (TPU) Et team af kemikere fra Tomsk Polytekniske Universitet opdagede en mekanisme for direkte elektrofil aminering
- Hvad kan der ske med lysenergi, der rejser gennem luften, når det møder et nyt stof.?
- Dage efter at have købt Time Warner, AT&T lancerer ny tv-tjeneste
- Kan en elektrisk strøm generere elektromagnetiske bølger?
- Verdens første metal 3-D-printede bro går i testfase
- I processen med havbund spreder sig, hvad der sker, når magma stiger op til jordoverfladen og stør…
- Hvilke biome har træer, der kan stå de kolde temperaturer?


