Videnskaben bag vands hydrogenbinding
Af Diane EvansOpdateret 30. august 2022
Vand indeholder to forskellige typer bindinger:kovalente bindinger, der holder oxygen- og hydrogenatomerne sammen inden for hvert molekyle, og hydrogenbindinger, der forbinder et vandmolekyle til et andet. De kovalente bindinger giver vand dets molekylære struktur, mens brintbindingerne skaber det netværk, der definerer væskens bulkegenskaber.
Brintbinding i flydende vand
I flydende vand er hydrogenbindinger relativt svage, men deres store antal dominerer molekylets adfærd. De opstår fra elektrostatisk tiltrækning mellem de delvist positive brintatomer og de delvist negative oxygenatomer. Fordi molekylerne konstant er i bevægelse, dannes og brydes disse bindinger dynamisk. Opvarmning øger den molekylære kinetiske energi, styrker tendensen til bindinger til at bryde og tillader vand at fordampe. I den gasformige fase driver vandmolekyler uafhængigt; når de er afkølet, genetableres hydrogenbindinger, og væsken gendannes.
Brintbinding i is
Is vedtager et krystallinsk gitter, hvor hvert vandmolekyle er tetraedrisk koordineret af fire naboer gennem hydrogenbindinger. Dette ordnede arrangement begrænser molekylær bevægelse, hvilket gør is mindre tæt end flydende vand. Som et resultat flyder isen og danner et beskyttende tæppe over vandmasser, der understøtter livet i vand om vinteren.
Vand som opløsningsmiddel
Vands polaritet - en ujævn fordeling af ladning forårsaget af det elektronegative oxygenatom - gør det muligt for det at omgive og adskille ioner og polære molekyler. Den lille størrelse af vandmolekyler lader mange af dem samle sig omkring et opløst stof og danner hydrogenbindinger, der trækker det opløste stof fra hinanden. Dette forklarer, hvorfor vand opløser flere stoffer end nogen anden væske, hvilket giver sin titel som det "universelle opløsningsmiddel."
Vands fysiske egenskaber
Hydrogenbinding giver høj kohæsion og overfladespænding, tydeligt når dråber perler på voksede overflader. Det står også for vands høje fordampningsvarme, hvilket gør sveden til en effektiv kølemekanisme for pattedyr. Den store energi, der kræves for at bryde brintbindinger, betyder, at vand forbliver flydende over et bredt temperaturområde, hvilket understøtter livets processer.
Brintbinding i biologiske systemer
Ud over selvinteraktion binder vand hydrogen til molekyler, der besidder hydroxyl- (OH)- eller amin- (NH₂)-grupper, en egenskab, der er afgørende for utallige biokemiske reaktioner. Vands evne til at stabilisere strukturer og transportere molekyler, kombineret med dets termiske bufferkapacitet, har været uundværlig for udviklingen af livet på Jorden.
 Varme artikler
Varme artikler
-
 Forskere koder Wizard of Oz i en forsvindende lille plastikForskere gemte data i den kemiske struktur af en polymer, blandede dem i blækket i et personligt brev, sendte det med post og var i stand til at hente en kompleks krypteringsnøgle og dekryptere en kop
Forskere koder Wizard of Oz i en forsvindende lille plastikForskere gemte data i den kemiske struktur af en polymer, blandede dem i blækket i et personligt brev, sendte det med post og var i stand til at hente en kompleks krypteringsnøgle og dekryptere en kop -
 Forskere afslører virkningsmekanisme for lovende kræftforbindelseUNC Linebergers Lee M. Graves, PhD. Kredit:University of North Carolina ved Chapel Hill School of Medicine Forskere fra University of North Carolina Lineberger Comprehensive Cancer Center har afsl
Forskere afslører virkningsmekanisme for lovende kræftforbindelseUNC Linebergers Lee M. Graves, PhD. Kredit:University of North Carolina ved Chapel Hill School of Medicine Forskere fra University of North Carolina Lineberger Comprehensive Cancer Center har afsl -
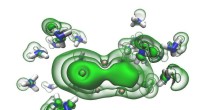 Et forsøg foreslået af en ph.d. elev kan omskrive kemi lærebøgerSolvatiserede elektroner (grønne) i hullerne mellem ammoniakmolekyler (blå og hvide) begynder at smelte sammen til et par, efterhånden som en opløsning bevæger sig mod at blive metallisk. Kredit:Ryan
Et forsøg foreslået af en ph.d. elev kan omskrive kemi lærebøgerSolvatiserede elektroner (grønne) i hullerne mellem ammoniakmolekyler (blå og hvide) begynder at smelte sammen til et par, efterhånden som en opløsning bevæger sig mod at blive metallisk. Kredit:Ryan -
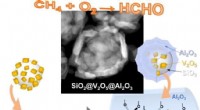 Forskere finder nye måder at udnytte spildt metan påSkematisk billede, der viser SiO 2 @V 2 O 5 @Al 2 O 3 core@shell nanostrukturer. Kredit:UNIST Den primære komponent i naturgas, metan, er i sig selv en potent drivhusgas. En nylig unders
Forskere finder nye måder at udnytte spildt metan påSkematisk billede, der viser SiO 2 @V 2 O 5 @Al 2 O 3 core@shell nanostrukturer. Kredit:UNIST Den primære komponent i naturgas, metan, er i sig selv en potent drivhusgas. En nylig unders
- Hvad ville virkningen være på plante- og dyreceller, hvis der ikke blev eksisterende vand?
- Japans Hitachi fryser britisk atomprojekt
- Hvad er forbindelserne af radium?
- Hvad har mere intern energi 25 kg vand eller guld ved termisk ligevægt?
- Hvorfor dit hår og dine negle ikke vokser efter døden:Aflivning af myten
- En studerende konverterede forkert 20ºC til 64ºF i stedet for 68ºF Hvad er den omtrentlige procen…


