Mestring af støkiometri:En trin-for-trin guide til nøjagtige beregninger
Af Jack Brubaker – Opdateret 30. august 2022
Støkiometri beskriver de kvantitative forhold mellem reaktanter og produkter i en kemisk reaktion. Selvom konceptet er grundlæggende for kemi, kæmper mange elever med de tilhørende muldvarp-baserede beregninger. Nøglen til at mestre støkiometri ligger i en systematisk, fem-trins tilgang, der forenkler selv de mest komplekse problemer.
Trin 1:Balancer ligningen
Begynd med at afbalancere den kemiske ligning, så hvert atom vises på begge sider af pilen. For eksempel balancerer reaktionen mellem hydrogengas (H₂) og oxygengas (O₂) for at producere vand (H₂O) som:
2 H₂ + O₂ → 2 H₂O
Denne afbalancerede form fortæller os, at to brintmolekyler reagerer med et iltmolekyle for at generere to vandmolekyler.
Trin 2:Konverter masse til mol
Omdan den kendte masse af en enkelt komponent til mol ved at dividere med dens molære masse. Muldvarpe er en bekvem enhed, der tillader sammenligning af forskellige stoffer uanset deres masse. Hvis du f.eks. starter med 1,0 g H₂, er beregningen:
(1.0 g) ÷ (2.02 g mol⁻¹) = 0.50 mol H₂
Trin 3:Anvend det støkiometriske forhold
Brug koefficienterne fra den balancerede ligning til at finde mol af andre arter. Forholdet er simpelthen koefficienten af målforbindelsen over koefficienten for den kendte forbindelse. Fra eksemplet:
- O₂ påkrævet:
0.50 mol × (1 ÷ 2) = 0.25 mol O₂ - H₂O produceret:
0.50 mol × (2 ÷ 2) = 0.50 mol H₂O
Trin 4:Konverter tilbage til masse
Oversæt molerne tilbage til gram ved at gange med den passende molære masse:
- O₂:
0.25 mol × 32.00 g mol⁻¹ = 8.0 g O₂ - H₂O:
0.50 mol × 18.02 g mol⁻¹ = 9.0 g H₂O
Trin 5:Bekræft massekonservering
Bekræft, at den samlede masse af reaktanter er lig med den samlede masse af produkter, i overensstemmelse med loven om bevarelse af masse. I dette tilfælde er 1,0 gH₂ + 8,0 gO₂ = 9,0 g, hvilket svarer til 9,0 gH₂O produceret.
Ting, du skal bruge
- Videnskabelig lommeregner
- Periodisk tabel (til nøjagtige atommasser)
Følg denne kortfattede metode, og støkiometri bliver en forudsigelig, gentagelig proces snarere end en skræmmende beregning.
 Varme artikler
Varme artikler
-
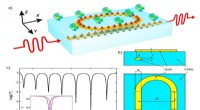 Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi
Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi -
 Sådan laver du en 1:4-fortynding:Bland en del koncentrat med fire dele vandAf Melissa Mayer Opdateret 30. august 2022 Irina Vodneva/iStock/GettyImages Fra husholdningsrengøringsmidler til laboratorieprøver er simple fortyndinger overalt. At mestre fortyndingsforhold giver
Sådan laver du en 1:4-fortynding:Bland en del koncentrat med fire dele vandAf Melissa Mayer Opdateret 30. august 2022 Irina Vodneva/iStock/GettyImages Fra husholdningsrengøringsmidler til laboratorieprøver er simple fortyndinger overalt. At mestre fortyndingsforhold giver -
 Sveden er en eksoterm proces, der holder os køligegorodenkoff/iStock/GettyImages Sveden er en naturlig reaktion på varme, fysisk anstrengelse eller følelsesmæssig stress. Når vores kropstemperatur stiger, udløser nervesystemet svedkirtlerne til at f
Sveden er en eksoterm proces, der holder os køligegorodenkoff/iStock/GettyImages Sveden er en naturlig reaktion på varme, fysisk anstrengelse eller følelsesmæssig stress. Når vores kropstemperatur stiger, udløser nervesystemet svedkirtlerne til at f -
 En bedre måde at opdele vandmolekyler for at producere brint ved hjælp af sollysTransmissionselektronmikroskopi. en, b, Valgt område-elektrondiffraktionsmønster opnået fra SrTiO3:Al ladet med Rh (0,1 vægt-%)/Cr2O3 (0,05 vægt-%)/CoOOH (0,05 vægt-%) (a) og tilsvarende transmissions
En bedre måde at opdele vandmolekyler for at producere brint ved hjælp af sollysTransmissionselektronmikroskopi. en, b, Valgt område-elektrondiffraktionsmønster opnået fra SrTiO3:Al ladet med Rh (0,1 vægt-%)/Cr2O3 (0,05 vægt-%)/CoOOH (0,05 vægt-%) (a) og tilsvarende transmissions
- Sådan skrives kemiske formler til overgangsmetaller
- Ny indsigt i, hvorfor Pierces sygdom er så dødelig for vinstokke
- Hvilken mængde giver både objektets hastighed og retning?
- Hvad er 3 måder at overføre energi på?
- Vandtankskibe viser en redningslinje for indias udtørrede landsbyer
- Undersøgelse forbinder unges syn på politiet med sandsynligheden for aggressiv adfærd


