Beregning af muldvarpe nødvendige for en kemisk reaktion:En praktisk støkiometriguide
Af Jack Brubaker – Opdateret 30. august 2022
I hvert laboratorium udfører kemikere præcise beregninger for at bestemme de nøjagtige mængder af reaktanter og produkter, der kræves til en given reaktion. Denne disciplin, kendt som støkiometri, er afhængig af begrebet muldvarpen – en grundlæggende enhed, der repræsenterer 6,022×10 23 formelenheder for et stof. Molen er defineret således, at et mol af en forbindelse vejer præcis dens formelvægt i gram, hvor formelvægten er summen af atomvægtene af alle atomer i molekylformlen. For eksempel har natriumchlorid (NaCl) en formelvægt på 58,44 gmol -1 , hvilket betyder, at 58,44 g NaCl indeholder 6,022×10 23 formelenheder.
Trin 1:Skriv en afbalanceret kemisk ligning
Start med at udarbejde en afbalanceret ligning for reaktionen af interesse. En afbalanceret ligning indeholder det samme antal af hver type atom på begge sider af pilen. For eksempel reaktionen mellem calciumhydroxid (Ca(OH)2 ) og saltsyre (HCl) skrives som:
Ca(OH)2 + HCl → CaCl2 + H2 O
Denne version er ubalanceret:venstre side har to oxygenatomer og et kloratom, mens højre side har to kloratomer og et oxygenatom. Den korrekt afbalancerede ligning er:
Ca(OH)2 + 2HCl → CaCl2 + 2H2 O
Nu vises hvert element i lige mange på begge sider.
Trin 2:Bestem formelvægte
Beregn derefter formelvægten af hver forbindelse i den afbalancerede ligning. Formelvægt opnås ved at summere atomvægtene af alle tilstedeværende atomer. For eksempel calciumchlorid (CaCl2 ) indeholder et calciumatom (40,08 gmol -1 ) og to kloratomer (35,45 gmol -1 hver), hvilket giver:
(1×40,08) + (2×35,45) =100,98 gmol -1
Trin 3:Konverter kendt masse til mol
Når du kender massen af en reaktant eller et produkt, skal du konvertere denne masse til mol ved at dividere med dens formelvægt. Brug den afbalancerede reaktion ovenfor, antag, at du har 10 g calciumhydroxid. Formelvægten af Ca(OH)2 er 74,10 gmol -1 , så molerne af Ca(OH)2 tilstedeværende er:
10g÷74,10gmol ‑1 =0,135 mol (≈0,13 mol)
Trin 4:Anvend det støkiometriske forhold
Brug koefficienterne fra den balancerede ligning til at relatere de kendte mol til de ukendte mol. I Ca(OH)2 + 2HCl → CaCl2 + 2H2 O, det støkiometriske forhold mellem HCl og Ca(OH)2 er 2:1. Derfor:
0,135 molCa(OH)2 ×(2molHCl÷1molCa(OH)2 ) =0,270 molHCl
Der kræves således 0,270 mol HCl for at reagere fuldstændigt med 10 g Ca(OH)2 .
Nødvendige materialer
- Periodisk tabel over grundstoffer (for atomvægte)
- Videnskabelig lommeregner (til division og multiplikation)
Ved at følge disse systematiske trin kan du nøjagtigt bestemme de molmængder, der er nødvendige for enhver kemisk reaktion, hvilket sikrer præcise støkiometriske beregninger i laboratoriet.
 Varme artikler
Varme artikler
-
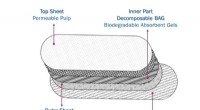 Sikrere hygiejnebind lavet af palmestivelseSkematisk af det fremstillede biologisk nedbrydelige hygiejnebind. Kredit:International Islamic University Malaysia Et biologisk nedbrydeligt hygiejnebind lavet af sagostivelse kunne bidrage til i
Sikrere hygiejnebind lavet af palmestivelseSkematisk af det fremstillede biologisk nedbrydelige hygiejnebind. Kredit:International Islamic University Malaysia Et biologisk nedbrydeligt hygiejnebind lavet af sagostivelse kunne bidrage til i -
 Størrelse betyder noget, når det kommer til atomare egenskaberEn illustration af kaliumatomer, der undergår ændringer i fundamentale egenskaber såsom radius, energi og elektronegativitet, da de komprimeres af omgivende neonatomer Kredit:Neuroncollective, Daniel
Størrelse betyder noget, når det kommer til atomare egenskaberEn illustration af kaliumatomer, der undergår ændringer i fundamentale egenskaber såsom radius, energi og elektronegativitet, da de komprimeres af omgivende neonatomer Kredit:Neuroncollective, Daniel -
 Hvordan forhøjet temperatur påvirker eksoterme reaktioner:hastighed, ligevægt og praktiske konsek…Emilija Randjelovic/iStock/GettyImages I kemi er eksoterme reaktioner dem, der frigiver varme til deres omgivelser. Når temperaturen i et sådant system hæves, opstår der to primære effekter:reaktions
Hvordan forhøjet temperatur påvirker eksoterme reaktioner:hastighed, ligevægt og praktiske konsek…Emilija Randjelovic/iStock/GettyImages I kemi er eksoterme reaktioner dem, der frigiver varme til deres omgivelser. Når temperaturen i et sådant system hæves, opstår der to primære effekter:reaktions -
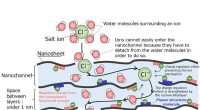 Meget funktionel membran udviklet til fremstilling af ferskvand fra havvandDiagram af membranen. Vandgennemtrængning induceres af nanokanalerne. Det er svært for ionerne at komme ind i nanokanalerne, så de kan ikke let trænge igennem membranen. Kredit:Kobe University Pro
Meget funktionel membran udviklet til fremstilling af ferskvand fra havvandDiagram af membranen. Vandgennemtrængning induceres af nanokanalerne. Det er svært for ionerne at komme ind i nanokanalerne, så de kan ikke let trænge igennem membranen. Kredit:Kobe University Pro
- Hvilke mineraler findes i Rusland?
- Hvad er forholdet mellem carbonatomer og brint i et molekyle -oktan?
- Skovbrande raser i Grækenland, truer OL's fødested
- Hvad er de mest almindelige mineraler i jordskorpe?
- En halv grad mindre opvarmning kan undgå ekstreme nedbørsmængder
- Udforsk den skjulte skønhed ved sommerfuglevinger under et mikroskop


