Sådan beregnes det andet ækvivalenspunkt i en titrering
Af John Brennan
Opdateret 30. august 2022
En titrering er en klassisk laboratorieteknik, der bruges til at bestemme koncentrationen af et stof i opløsning. Syre-base titreringer, hvor en syre og en base neutraliserer hinanden, er de hyppigste. Det punkt, hvor al syre eller base i analytten er blevet neutraliseret, kaldes ækvivalenspunktet. For diprotiske syrer eller baser forekommer der også et andet ækvivalenspunkt, og beregning af pH på dette tidspunkt er ligetil med de rigtige data.
Trin 1
Identificer analyttens natur (syre eller base), den specifikke type (f.eks. oxalsyre) og dens koncentration og volumen. I lektieopgaver gives denne information; i et laboratorium optager du det, mens du titrerer.
Trin 2
Diprotiske arter - dem, der kan donere eller acceptere mere end én proton - udviser et andet ækvivalenspunkt. Hent den anden dissociationskonstant (Ka2 for syrer eller Kb2 for baser) fra en pålidelig kilde, såsom en standard referencetekst eller en velrenommeret onlinedatabase.
Trin 3
Beregn det samlede antal mol af analytten. Gang dens molaritet med dens volumen (i liter). For eksempel indeholder 40mL 1M oxalsyre:
(0,040L × 1molL⁻¹) =0,04mol.
Trin 4
Bestem det endelige volumen ved at tilføje titrantvolumenet til det originale analytvolumen. I eksemplet giver 80mL 1M NaOH tilsat 40mL 1M oxalsyre 120mL i alt.
Trin 5
Beregn koncentrationen af den konjugerede art ved det andet ækvivalenspunkt:
0,04mol ÷ 0,120L =0,333M.
Trin 6
Bestem Kb af den fuldt deprotonerede konjugatbase (eller Ka af den konjugerede syre). For en diprotisk syre, Kb =1×10⁻¹⁴ ÷ Ka2 . Brug af oxalsyre (Ka2 =5,4 x 10⁻⁵):
1×10⁻¹⁴ ÷ 5,4×10⁻⁵ =1,852×10⁻¹⁰.
Trin 7
Indstil basisligevægtsudtrykket:
Kb =([OH⁻][konjugatsyre])/[konjugatbase].
Trin 8
Forudsat at ændringen i koncentrationen er lille, lad x repræsentere [OH⁻] og [konjugatsyre]. Ligningen bliver:
1,852×10⁻¹⁰ =x² ÷ 0,333.
Løsning:x² =6,167×10⁻¹¹ → x =7,85×10⁻⁶M.
Trin 9
Konverter hydroxidkoncentrationen til pH. Find først pOH =–log₁₀(7,85×10⁻⁶) =5,105. Derefter er pH =14 – pOH =8,90.
Trin 10
Således er pH ved det andet ækvivalenspunkt 8,90.
Ting, der er nødvendige
- Blyant
- Papir
- Lommeregner
TL;DR (for lang; læste ikke)
Denne beregning udelader vandautoionisering, som kan påvirke meget fortyndede opløsninger af svage baser eller syrer. Ikke desto mindre giver det et pålideligt skøn til de fleste praktiske formål.
 Varme artikler
Varme artikler
-
 Mestring af kemisk formelskrivning:En praktisk vejledningAdrian Hernandez/iStock/Getty Images Brug det periodiske system At skrive kemiske formler begynder med en solid forståelse af det periodiske system. Tabellen viser alle kendte grundstoffer og parrer
Mestring af kemisk formelskrivning:En praktisk vejledningAdrian Hernandez/iStock/Getty Images Brug det periodiske system At skrive kemiske formler begynder med en solid forståelse af det periodiske system. Tabellen viser alle kendte grundstoffer og parrer -
 Fund tilbyder opskrift på finjustering af legeringer til brug ved høj temperaturEt stykke legering er stresstestet i Levente Vitos laboratorium ved KTH Royal Institute of Technology. Kredit:Levente Vitos Superlegeringer, der tåler ekstremt høje temperaturer, kunne snart blive
Fund tilbyder opskrift på finjustering af legeringer til brug ved høj temperaturEt stykke legering er stresstestet i Levente Vitos laboratorium ved KTH Royal Institute of Technology. Kredit:Levente Vitos Superlegeringer, der tåler ekstremt høje temperaturer, kunne snart blive -
 Mærkelige ting sker, når en krystal er delt i toEn labyrintlignende struktur opstår på overfladen. Kredit:TU Wien Den bemærkelsesværdige styrke af ioniske krystaller er let forklaret på atomær skala:Positivt og negativt ladede atomer sidder sid
Mærkelige ting sker, når en krystal er delt i toEn labyrintlignende struktur opstår på overfladen. Kredit:TU Wien Den bemærkelsesværdige styrke af ioniske krystaller er let forklaret på atomær skala:Positivt og negativt ladede atomer sidder sid -
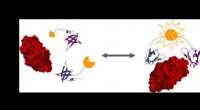 At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at
At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at
- Asteroider og kometer overfylder Mars med organiske stoffer
- Hvordan udføres varme gennem en glasvæg af vaccuumglas?
- Modsat handling kunne forbedre industriel gasseparation
- Hvor er alle vandfontænerne blevet af? Her er hvorfor vi bør bringe dem tilbage
- Hvad er frekvensen i MHz af en stråle blåt lys, hvis bølgelængde er 4000 Ångströms?
- Hvorfor krom har et højt kogepunkt?


