Eksergoniske vs. endergoniske reaktioner:Vigtigste forskelle forklaret
I kemi er reaktioner kategoriseret efter, hvordan de håndterer energi. Eksergoniske reaktioner frigive energi – typisk som varme eller lys – mens endergoniske reaktioner forbruge energi for at fortsætte.
Typiske eksempler
Forbrænding af benzin er en klassisk eksergonisk reaktion. Oktanmolekyler i benzin indeholder mere kemisk energi end det producerede vand og kuldioxid, så der frigives energi, når brændstoffet brænder. I modsætning hertil er fotosyntese i træer en endergonisk proces, der lagrer energi ved at omdanne kuldioxid og vand til komplekse organiske molekyler som cellulose.
Biologisk betydning
Organismer er stærkt afhængige af endergoniske reaktioner for at opbygge essentielle biomolekyler såsom aminosyrer, nukleotider og fedtstoffer. Disse processer trækker energi fra sukkerarter eller andre højenergisubstrater. Fordi endergoniske reaktioner ikke kan forløbe spontant, leverer celler den nødvendige energi via ATP eller andre co-enzymer.
Aktiveringsenergi
Selv eksergoniske reaktioner kræver ofte et første input af energi - kendt som aktiveringsenergi - for at overvinde kinetiske barrierer. Trækul har for eksempel brug for en gnist eller en tændstik for at antænde. Når først reaktionen er udløst, frigives den lagrede aktiveringsenergi, og reaktionen fortsætter og frigiver mere energi, end der oprindeligt blev investeret.
Vendbarhed
Endergoniske reaktioner er ofte reversible. For eksempel vender afbrænding af en træstamme den fotosynteseproces, der oprindeligt dannede træet:Kulhydrater oxideres til CO₂ og H₂O, hvilket frigiver en beskeden mængde varme. Vanskeligheden ved at vende en eksergonisk reaktion afhænger af, hvor meget yderligere energi der kræves for at drive den omvendte proces. Dette koncept understreges af forskning fra University of Nebraska, Lincoln.
Energy Hill Diagram
Et energibakkediagram repræsenterer visuelt energiprofilen af en reaktion. Den vandrette akse viser reaktionskoordinaten (tid eller fremskridt), mens den lodrette akse viser systemets samlede energi. For en eksergonisk reaktion stiger diagrammet til et højdepunkt - der repræsenterer aktiveringsenergien - og falder derefter under det oprindelige energiniveau. For en endergonisk reaktion stiger stien over startenergien, hvilket indikerer, at systemet skal absorbere energi, før reaktionen kan fuldføres.
 Varme artikler
Varme artikler
-
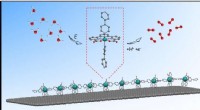 Oligomere materialer for at forbedre vandspaltningOligomer katalysator. Kredit:Marcos Gil-Sepulcre (ICIQ) Forskere fra Llobet-gruppen har udviklet et nyt molekylært materiale lavet af oligomerer og brugt det som en katalysator i vandoxidation, op
Oligomere materialer for at forbedre vandspaltningOligomer katalysator. Kredit:Marcos Gil-Sepulcre (ICIQ) Forskere fra Llobet-gruppen har udviklet et nyt molekylært materiale lavet af oligomerer og brugt det som en katalysator i vandoxidation, op -
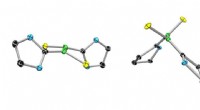 Generering af en stabil biradicalEn konventionel bor-bor dobbeltbinding (venstre) og dens ekstremt stabile biradiske slægtning. Kredit:Dr. Rian Dewhurst Bor har en række anvendelser, fra vaskeblegemiddel til varmebestandigt glas
Generering af en stabil biradicalEn konventionel bor-bor dobbeltbinding (venstre) og dens ekstremt stabile biradiske slægtning. Kredit:Dr. Rian Dewhurst Bor har en række anvendelser, fra vaskeblegemiddel til varmebestandigt glas -
 Undersøgelsen sigter mod at øge antitumoral aktivitet af forbindelse ekstraheret fra en Amazon-pla…Uncaria guianensis, i flor, Cacuri, Venezuela. CC3.0 Forskere i Brasilien har udarbejdet modificerede former af alkaloiderne produceret af Uncaria guianensis , en træagtig vin, der er hjemmehøre
Undersøgelsen sigter mod at øge antitumoral aktivitet af forbindelse ekstraheret fra en Amazon-pla…Uncaria guianensis, i flor, Cacuri, Venezuela. CC3.0 Forskere i Brasilien har udarbejdet modificerede former af alkaloiderne produceret af Uncaria guianensis , en træagtig vin, der er hjemmehøre -
 Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred
Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred


