Når en cofaktor mangler:Hvorfor enzymer ikke katalyserer reaktioner
Andy Sotiriou/Photodisc/Getty Images
Enzymer accelererer specifikke kemiske reaktioner, men mange kræver en cofaktor - en ikke-proteinion eller et molekyle - for at udføre deres funktion. Når en cofaktor er fraværende, mister enzymet sin katalytiske evne, hvilket gør reaktionen ineffektiv.
Funktion
En cofaktor er en essentiel ikke-protein-komponent, der gør det muligt for et enzym at katalysere sin reaktion. Fjernelse af cofaktoren standser enzymets aktivitet. For eksempel omdanner kulsyreanhydrase i humant blod vand og kuldioxid til kulsyre; det kræver en zinkion for at binde vand og lette reaktionen. Uden zink bliver kulsyreanhydrase inaktiv.
Typer
Kofaktorer findes i to hovedvarianter:
- Metalioner såsom jern, magnesium og zink.
- Små organiske molekyler som vitamin B12, der ofte fungerer som coenzymer.
Mange vitaminer tjener som enzym-cofaktorer eller prækursorer. Nogle cofaktorer er tæt bundet og bliver integrerede dele af enzymet, kendt som protesegrupper, mens andre binder løst.
Mekanisme
Rollen af en cofaktor afhænger af enzymets katalytiske mekanisme. I kulsyreanhydrase sidder zinkionen i kløften på det aktive sted og tiltrækker et vandmolekyle. Dens positive ladning stabiliserer dannelsen af en hydroxidion, som derefter angriber kuldioxid for at danne kulsyre. Ved at muliggøre tab af en hydrogenion fra vand, driver zink direkte reaktionen.
Applikationer
Forsætlig fjernelse af en cofaktor er en almindelig strategi til at hæmme uønsket enzymatisk aktivitet. I molekylærbiologi chelaterer EDTA magnesiumioner, hvilket gør DNaser inaktive og beskytter ekstraheret DNA. På samme måde retter mange antibiotika sig mod bakterielle enzymer ved at binde eller fortrænge essentielle metalcofaktorer.
 Varme artikler
Varme artikler
-
 Anatomi af en acnebehandlingKredit:CC0 Public Domain Sarecyclin, et lægemiddel godkendt til brug i USA i 2018, er det første nye antibiotikum godkendt til behandling af acne i mere end 40 år. Nu, forskere ved Yale og Univers
Anatomi af en acnebehandlingKredit:CC0 Public Domain Sarecyclin, et lægemiddel godkendt til brug i USA i 2018, er det første nye antibiotikum godkendt til behandling af acne i mere end 40 år. Nu, forskere ved Yale og Univers -
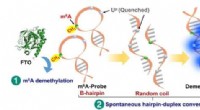 Ny probe for stofskiftesygdommeFigur viser analysestrategien til påvisning af FTO -niveauer i celler. Fjernelse af methylgruppen med FTO udløser en omstilling fra en hårnål til en dupleksstruktur, forårsager fluorescens. Billedet (
Ny probe for stofskiftesygdommeFigur viser analysestrategien til påvisning af FTO -niveauer i celler. Fjernelse af methylgruppen med FTO udløser en omstilling fra en hårnål til en dupleksstruktur, forårsager fluorescens. Billedet ( -
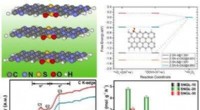 Forskere indser effektiv hydrogenperoxidproduktion i syreIllustration af forskningen. Kredit:Prof. Guans gruppe Som et af de 100 vigtigste kemikalier i verden er hydrogenperoxid (H2 O2 ) fremstilles hovedsageligt ved den energi- og affaldsintensive anthr
Forskere indser effektiv hydrogenperoxidproduktion i syreIllustration af forskningen. Kredit:Prof. Guans gruppe Som et af de 100 vigtigste kemikalier i verden er hydrogenperoxid (H2 O2 ) fremstilles hovedsageligt ved den energi- og affaldsintensive anthr -
 Hollandsk dronning og robot åbner 3D-printet bro i AmsterdamEn 3D-printet fodgængerbro spænder over en kanal i hjertet af red light district i Amsterdam, Holland, Torsdag, 15. juli, 2021. De karakteristiske flydende linjer på 12 meter (40 fod) broen blev skabt
Hollandsk dronning og robot åbner 3D-printet bro i AmsterdamEn 3D-printet fodgængerbro spænder over en kanal i hjertet af red light district i Amsterdam, Holland, Torsdag, 15. juli, 2021. De karakteristiske flydende linjer på 12 meter (40 fod) broen blev skabt
- eBays nye Managed Delivery har til formål at konkurrere med Amazon
- I hvilket område af jordens indre stiger varmen til at pege på, at sten begynder at smelte?
- På forkant med at udvikle ny indsigt i fredsopbygning
- Miljø, der imødekommer en organismeens behov?
- Hvad er et eksempel på en planetarisk tåge?
- Hvad er et iørefaldende videnskabsmæssigt projektnavn?


