Hvorfor molær masse betyder noget i kemi:En praktisk vejledning
Af Jason Thompson, Opdateret 30. august 2022
Når du skal vurdere, hvor meget af et stof du har brug for, kan vægt eller volumen alene være vildledende. Densitetsvariationer betyder, at en tung, kompakt genstand kan indeholde langt færre molekyler end en let, porøs en. Kemikere overvinder dette ved at bruge muldvarpen , en enhed, der tæller partikler i stedet for masse eller rum. En muldvarp svarer til ca. 6,022×10 23 atomer, molekyler eller ioner.
Definition
Molar masse er massen af et mol af et stof, udtrykt i gram pr. mol (gmol -1 ). Det er forholdet mellem massen af en prøve og antallet af partikler, den indeholder. At kende molmassen giver dig mulighed for at konvertere mellem gram og mol med en simpel multiplikation eller division.
Eksperimentel opsætning
Nøjagtige målinger afhænger af den korrekte mængde reaktant. For eksempel, hvis en protokol kræver 2 mol rent kulstof, beregner du den nødvendige masse som følger:
- Molar masse af kulstof =12,01 gmol -1
- 2mol×12,01gmol -1 =24,02 g
En vægt på 24,02 g kulstof sikrer, at reaktionen modtager den nøjagtige støkiometriske mængde.
Eksperimentel analyse
Sammenligning af de volumener, der optages af lige store molmængder af forskellige stoffer, afslører indsigt om molekylstørrelse og pakning. Hvis 1 mol af stof A optager et større volumen end 1 mol af stof B, er molekylerne af A sandsynligvis større eller mindre effektivt pakket.
Masseprocentberegninger
Molær masse hjælper med at bestemme bidraget fra hvert element til en forbindelses samlede masse. Tag 28,00 g kulilte (CO) som eksempel:
- Molar masse af kulstof =12,01 gmol -1
- Molar masse af oxygen =16,00 gmol -1
- Total molær masse af CO =12,01+16,00=28,01gmol -1
- Carbons massefraktion =(12,01/28,01)×100=42,89 %
Kulstof udgør således 42,89 % af CO’s masse.
Forudsigelse af molære masser
Når en ny forbindelse syntetiseres, kan dens molære masse beregnes uden laboratoriemåling ved at summere de molære masser af dets konstituerende atomer. Denne forudsigende tilgang strømliner reagensfremstilling og støkiometriske beregninger.
 Varme artikler
Varme artikler
-
 En ny måde at se stress på - ved hjælp af supercomputereSupercomputersimuleringer viser, at på atomniveau, materiel stress opfører sig ikke symmetrisk. Molekylær model af en krystal, der indeholder en dissocieret dislokation, atomer er kodet med atomforsky
En ny måde at se stress på - ved hjælp af supercomputereSupercomputersimuleringer viser, at på atomniveau, materiel stress opfører sig ikke symmetrisk. Molekylær model af en krystal, der indeholder en dissocieret dislokation, atomer er kodet med atomforsky -
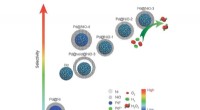 Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred -
 For at lave aminosyrer, tilføj bare elektricitetEn demonstrationsflowreaktor konstrueret af forskere ved Kyushu University omdanner løbende kildematerialer til aminosyrer gennem en reaktion drevet af elektricitet. Ved at vælge den rigtige kombinati
For at lave aminosyrer, tilføj bare elektricitetEn demonstrationsflowreaktor konstrueret af forskere ved Kyushu University omdanner løbende kildematerialer til aminosyrer gennem en reaktion drevet af elektricitet. Ved at vælge den rigtige kombinati -
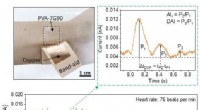 Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue
Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue
- Forskere modellerer Mercurys gletsjere
- Hvilket navn gives til et underjordisk hul dannet ved opløsning af kalkstenens regnvand?
- Hvad styrede kredsløbet?
- Hvor lang tid tager det en M-type stjerne at nå hovedsekvensen sammenlignet som din sol?
- Er smeltning af en proces for at tilføje varmeenergi miljøet?
- Røntgenlaser udforsker, hvordan man skriver data med lys


