Nøgleforskelle mellem ioniske og kovalente forbindelser
Af Doug Leenhouts | Opdateret 30. august 2022
JVisentin/iStock/GettyImages
Når atomer binder, bestemmer den resulterende struktur - hvad enten det er kovalent eller ionisk - forbindelsens fysiske og kemiske adfærd. Vand er for eksempel et kovalent molekyle dannet af to brintatomer, der deler elektroner med et oxygenatom. At forstå disse bindinger er afgørende for at forudsige egenskaber såsom smeltepunkt, opløselighed og reaktivitet.
Kovalente forbindelser
Kovalente bindinger dannes udelukkende mellem ikke-metalatomer, der har lignende elektronegativiteter. Fordi hvert atom deler et eller flere elektronpar, er de resulterende molekyler normalt væsker eller gasser ved stuetemperatur og har lave smelte- og kogepunkter. Disse forbindelser er ofte let polære, og formen af molekylet er defineret af arrangementet af delte elektronpar.
En vigtig tommelfingerregel er, at når elektronegativitetsforskellen mellem to atomer er mindre end 1,7, er bindingen kovalent. Dannelsen af en kovalent binding frigiver energi, hvilket gør forbindelsen mere stabil, efterhånden som yderligere kovalente bindinger dannes.
Ioniske forbindelser
Ioniske forbindelser opstår, når et metal donerer en eller flere elektroner til et ikke-metal, hvilket skaber positivt og negativt ladede ioner, der tiltrækker hinanden. En elektronegativitetsforskel større end 1,7 indikerer typisk ionisk karakter. Disse faste stoffer udviser høje smelte- og kogepunkter og er meget polære, hvilket afspejler den betydelige ladningsadskillelse.
Eksempler på kovalente bindinger
Mange organiske molekyler er kovalent bundet, såsom metan (CH4), hvor et carbonatom deler elektroner med fire hydrogenatomer. Kovalente bindinger kan også eksistere mellem identiske atomer - oxygen (O₂), nitrogen (N₂) og chlor (Cl2) er alle diatomiske gasser. Sådanne bindinger kræver betydelig energi for at bryde, hvilket understreger deres styrke. I det periodiske system er bindinger mellem ikke-metaller og halogener (gruppe 17) uvægerligt kovalente.
Eksempler på ioniske forbindelser
Natriumchlorid (NaCl), det velkendte bordsalt, er et eksempel på en ionisk forbindelse. Det opløses let i vand, fordi dets ioniske gitter let forstyrres af opløsningsmiddelmolekyler. Andre almindelige ioniske stoffer omfatter magnesiumoxid (MgO), kaliumchlorid (KCl), calciumoxid (CaO) og jern(III)oxid (Fe2O3). I hvert tilfælde opnår atomer en ædelgaskonfiguration ved at overføre eller acceptere elektroner, hvilket resulterer i et stabilt gitter.
 Varme artikler
Varme artikler
-
 Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner.
Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner. -
 Kemikere bringer blandede foldede proteiner til liveDen aluminiumoxid nanopartikel-assisteret enzym genfoldning proces er vist. Kredit:ITMO University Forskere fra ITMO University i Sankt Petersborg og Hebrew University i Jerusalem har fundet en må
Kemikere bringer blandede foldede proteiner til liveDen aluminiumoxid nanopartikel-assisteret enzym genfoldning proces er vist. Kredit:ITMO University Forskere fra ITMO University i Sankt Petersborg og Hebrew University i Jerusalem har fundet en må -
 Forskere finder en billigere måde at lave brintenergi ud af vandKredit:Shutterstock Brintdrevne biler kan snart blive mere end blot en nyhed, efter at et UNSW-ledet hold af forskere har demonstreret en meget billigere og bæredygtig måde at skabe den brint, der
Forskere finder en billigere måde at lave brintenergi ud af vandKredit:Shutterstock Brintdrevne biler kan snart blive mere end blot en nyhed, efter at et UNSW-ledet hold af forskere har demonstreret en meget billigere og bæredygtig måde at skabe den brint, der -
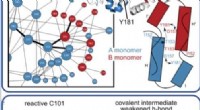 Forskere afslører, hvordan enzymbevægelser katalyserer reaktionerDenne illustration viser, hvordan et enzym bevæger sig og ændrer sig, når det katalyserer komplekse reaktioner og nedbryder organiske forbindelser. Kredit: Proceedings of the National Academy of Scien
Forskere afslører, hvordan enzymbevægelser katalyserer reaktionerDenne illustration viser, hvordan et enzym bevæger sig og ændrer sig, når det katalyserer komplekse reaktioner og nedbryder organiske forbindelser. Kredit: Proceedings of the National Academy of Scien


