Den afgørende rolle for gram-per-mol omdannelsesfaktoren i støkiometri
ViktorCap/iStock/GettyImages
Hvorfor er Gram-Per-Mole-faktoren vigtig
I enhver støkiometrisk beregning er omregningsfaktoren gram-per-mol (g/mol) den kerne, der omdanner teoretiske molforhold til håndgribelige massemængder. Ved at oversætte mol til gram kan kemikere præcist bestemme, hvor meget reaktant der kræves, undgå spild og med sikkerhed forudsige produktudbytte.
TL;DR
Gram-per-mol-faktoren lader kemikere konvertere afbalancerede mol-ligninger til massemængder i den virkelige verden, hvilket sikrer, at reaktionerne er fuldstændige, og at produkterne kvantificeres nøjagtigt.
Loven om messens bevarelse
Antoine Lavoisiers princip om, at masse hverken skabes eller ødelægges, understøtter al kemisk balancering. Hvert atom, der indgår i en reaktion, skal optræde i produkterne, hvilket garanterer, at en afbalanceret ligning afspejler det samme antal atomer på hver side.
Eksempel:Ubalanceret – H2SO4 + NaOH → Na2SO4 + H2O . Dette giver tre hydrogener til venstre og kun to til højre. Tilføjer en mere NaOH giver en balanceret ligning:H2SO4 + 2NaOH → Na2SO4 + 2H2O , der opfylder fredningsloven.
Fra mol til masse:Anvendelse af Gram-Per-Mole-faktoren
Mens en afbalanceret ligning fortæller os molforholdene, afslører den ikke de faktiske nødvendige masser. G/mol-værdierne (ofte opført i et periodisk system) bygger bro over dette hul.
Eksempel:2Na + 2H2O → 2NaOH + H2 . Her kombineres to mol natrium (23g/mol) og to mol vand (18g/mol) og producerer to mol natriumhydroxid (40g/mol) og et mol hydrogengas (2g/mol). Beregningen giver 46g Na, 36g H2 O, hvilket giver 80 g NaOH og 2 g H2 , der illustrerer massekonservering i aktion.
 Varme artikler
Varme artikler
-
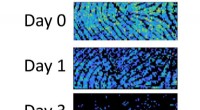 Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem.
Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem. -
 Mestring af vægt-for-volumen (w/v) beregninger for nøjagtige laboratorieløsningerAf Riti Gupta Opdateret 24. marts 2022 Totojang/iStock/GettyImages I laboratoriemiljøer kan opløsningskoncentrationen udtrykkes på flere måder. De mest almindelige udtryk er: Molaritet (M):mol opl
Mestring af vægt-for-volumen (w/v) beregninger for nøjagtige laboratorieløsningerAf Riti Gupta Opdateret 24. marts 2022 Totojang/iStock/GettyImages I laboratoriemiljøer kan opløsningskoncentrationen udtrykkes på flere måder. De mest almindelige udtryk er: Molaritet (M):mol opl -
 En ny metode til fremstilling af protoneret brintTrihydrogenioner (H + 3 ) kan dannes ved at udsætte vandmolekyler adsorberet til nanopartikler for intenst laserlys. Eksperimenterne efterligner de forhold, der findes i det ydre rum. Kredit:Ali A
En ny metode til fremstilling af protoneret brintTrihydrogenioner (H + 3 ) kan dannes ved at udsætte vandmolekyler adsorberet til nanopartikler for intenst laserlys. Eksperimenterne efterligner de forhold, der findes i det ydre rum. Kredit:Ali A -
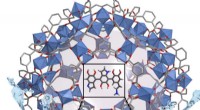 Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren
Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren


