Mestring af vægt-for-volumen (w/v) beregninger for nøjagtige laboratorieløsninger
Af Riti Gupta
Opdateret 24. marts 2022
Totojang/iStock/GettyImages
I laboratoriemiljøer kan opløsningskoncentrationen udtrykkes på flere måder. De mest almindelige udtryk er:
- Molaritet (M):mol opløst stof pr. liter opløsning (mol/L)
- Vægt-for-volumen (vægt/volumen):gram opløst stof pr. milliliter opløsning (g/ml)
- Vægt-for-vægt (vægt/vægt):gram opløst stof pr. gram opløsning (g/g)
- Volume-for-Volume (v/v):milliliter opløst stof pr. milliliter opløsning (mL/mL)
Denne artikel fokuserer på w/v-betegnelsen, som er særlig nyttig, når et tørt opløst stof vejes og opløses i et flydende opløsningsmiddel.
Hvorfor bruge W/V?
W/v foretrækkes, når du direkte kan måle massen af et fast reagens. For eksempel, hvis du vejer 5g KCl og opløser det i vand til et slutvolumen på 100mL, har du en 5% w/v KCl-opløsning. Koncentrationen er simpelthen massen af opløst stof divideret med opløsningens samlede volumen, udtrykt i procent.
Beregningen er:\(\mathrm{w/v\% =\frac{\text{masse af opløst stof i g}}{\text{volumen af opløsning i mL}} \ gange 100\%}\)
Forberedelse af løsninger med en mål W/V-koncentration
Antag, at du har brug for 100 ml af en 17 % w/v natriumazidopløsning. Ved at bruge formlen ovenfor:\(\mathrm{17\% =\frac{\text{masse af NaN}_3\text{ in g}}{100\text{ mL}} \time 100\%}\)
Løsning giver en nødvendig masse på 17 g natriumazid. Vej denne mængde og fortynd med vand for at nå 100 ml.
Omvendt, hvis du allerede har en opløsning, der indeholder 45g magnesiumacetat i et samlet volumen på 245mL, er vægt/volumenkoncentrationen:\(\mathrm{w/v\% =\frac{45\text{ g}}{245\text{ mL}} \time 100\% =18,4\>%}\)
W/v-beregninger undgår behovet for at bestemme muldvarpe, hvilket gør dem ligetil og effektive til rutinepræparater.Konvertering af W/V til Molaritet
Når der er givet en w/v-koncentration, og der kræves molaritet, skal du følge disse trin. Antag en 21% w/v NaCl-opløsning.
Bestem først massen af NaCl i 100mL:\(\mathrm{21\% =\frac{\text{masse af NaCl i g}}{100\text{ mL}} \times 100\%} \\Højrepil \text{masse af NaCl} =21\text{ g}\)
Omregn gram til mol ved hjælp af molmassen af NaCl (58,44 g/mol):\(\mathrm{\frac{21\text{ g NaCl}}{58,44\text{ g/mol}} =0,36\text{ mol NaCl}}\)
Til sidst beregnes molariteten ved at dividere mol med opløsningsvolumenet i liter (0,1L):\(\mathrm{\frac{0,36\text{ mol}}{0,1\text{ L}} =3,6\text{ M NaCl}}\)
En 21 % vægt/volumen NaCl-opløsning svarer således til en 3,6 M opløsning.
Ved at mestre m/v-beregninger og konverteringer kan du trygt udarbejde nøjagtige løsninger og oversætte koncentrationer på tværs af forskellige enheder.
Sidste artikelSådan testes surhedsgraden med lakmuspapir:en hurtig guide
Næste artikelVarier pH nøjagtigt for at måle enzymaktivitet
 Varme artikler
Varme artikler
-
 Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a
Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a -
 Forskere ser på meteoritter for at få inspiration til at opnå kritiske elementfri magnetThe Critical Materials Institute har udviklet en billig, højtydende permanentmagnet ved at hente inspiration fra en kilde, der ikke er af denne verden:jern-nikkel-legeringer i meteoritter. Kredit:U.S.
Forskere ser på meteoritter for at få inspiration til at opnå kritiske elementfri magnetThe Critical Materials Institute har udviklet en billig, højtydende permanentmagnet ved at hente inspiration fra en kilde, der ikke er af denne verden:jern-nikkel-legeringer i meteoritter. Kredit:U.S. -
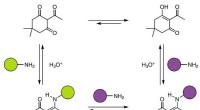 Kemikere fremstiller termohærdende polymer ved hjælp af amin og triketon, der kan genbrugesVendbar, dynamiske kovalente diketoenaminbindinger. Diketoenaminbindinger dannes spontant fra triketoner og både aromatiske og alifatiske aminer. Under stærkt sure forhold i vand, diketoenaminbindinge
Kemikere fremstiller termohærdende polymer ved hjælp af amin og triketon, der kan genbrugesVendbar, dynamiske kovalente diketoenaminbindinger. Diketoenaminbindinger dannes spontant fra triketoner og både aromatiske og alifatiske aminer. Under stærkt sure forhold i vand, diketoenaminbindinge -
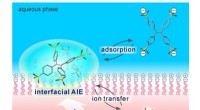 Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere
Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere
- Hvor i naturen forekommer stående bølger?
- Hvordan påvirker enkle maskiner kraftafstand gennem påført og retning?
- Hvordan forårsager rindende vandbølger og gletsjere erosionsaflejring?
- Hvor varmt kan Venus komme i sin atmosfære?
- Sådan finder du en tangentlinie til en Curve
- Hvad er baglæns og fremadrettet bevægelse af partikler i et fast stof kaldet?


