Sådan beregnes varmeabsorption:En praktisk vejledning
Af Lee Johnson
Opdateret 30. august 2022
MarianVejcik/iStock/GettyImages
TL;DR
Brug formlen Q =mcΔT at beregne varmeabsorberet.
- Q =varmeabsorberet (J)
- m =stoffets masse (kg)
- c =specifik varmekapacitet (Jkg⁻¹°C⁻¹)
- ΔT =ændring i temperatur (°C)
Termodynamiske fundamenter
Termodynamikkens første lov siger, at ændringen i indre energi i et system er lig med den varme, der tilføres det plus det arbejde, der udføres på det. Varme er en form for energioverførsel, der kun sker mellem kroppe ved forskellige temperaturer; det flyder spontant fra varmt til koldt. Forståelse af disse principper er afgørende for nøjagtige varmeberegninger.
Specifik varmekapacitet
Specifik varmekapacitet, betegnet c , kvantificerer, hvor meget energi der kræves for at hæve temperaturen på 1 kg af et materiale med 1°C. Typiske værdier omfatter:
- Vand:4181Jkg⁻¹°C⁻¹
- Bly:128Jkg⁻¹°C⁻¹
Beregning af varmeabsorption
Anvend den simple relation Q =mcΔT . Bestem først temperaturændringen:ΔT =T_final – T_initial.
Eksempel:Hæv 2 kg vand fra 10°C til 50°C.
- ΔT =50°C – 10°C =40°C
- Q =2kg × 4181Jkg⁻¹°C⁻¹ × 40°C =334480J (≈334,5kJ)
Enhedskonsistens og konvertering
Specifik varmekapacitet kan forekomme i alternative enheder:joule pr. gram pr. °C, kalorier pr. gram pr. °C eller joule pr. mol pr. °C. Hold enheder konsistente gennem hele beregningen. For eksempel, hvis c er angivet i Jg⁻¹°C⁻¹, brug masse i gram; hvis det er i Jmol⁻¹°C⁻¹, udtryk massen i mol. Temperaturforskelle målt i Kelvin er numerisk identiske med Celsius-forskelle, så ΔT kan bruges direkte.
Når du konverterer mellem energienheder, skal du huske:1kalorie =4,184J.
 Varme artikler
Varme artikler
-
 Hvordan reaktantmasse påvirker kemiske reaktionshastighederAf Diane Evans Opdateret 30. august 2022 Hastigheden af en kemisk reaktion er den hastighed, hvormed reaktanter omdannes til produkter. Kollisionsteori forklarer, at reaktioner kræver tilstrækkelig e
Hvordan reaktantmasse påvirker kemiske reaktionshastighederAf Diane Evans Opdateret 30. august 2022 Hastigheden af en kemisk reaktion er den hastighed, hvormed reaktanter omdannes til produkter. Kollisionsteori forklarer, at reaktioner kræver tilstrækkelig e -
 En ny form for cellulær logistikMin proteiner interagerer for at danne bølgemønstre (rød) og kan også transportere andre molekyler (blå) ved hjælp af diffusioforese. Kredit:Ramm et. al., Naturfysik 2021 Biofysikere fra Ludwig-Ma
En ny form for cellulær logistikMin proteiner interagerer for at danne bølgemønstre (rød) og kan også transportere andre molekyler (blå) ved hjælp af diffusioforese. Kredit:Ramm et. al., Naturfysik 2021 Biofysikere fra Ludwig-Ma -
 Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific
Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific -
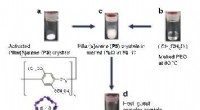 Valg af molekylvægtspolymer ved endimensionel indeslutningFigur 1. Vært-gæst kompleks dannelse mellem en krystal af aktiverede søjle[5]arener og en poly(ethylenoxid) smelte. Kredit:Kanazawa University Forskere ved Kanazawa University rapporterer i Natur
Valg af molekylvægtspolymer ved endimensionel indeslutningFigur 1. Vært-gæst kompleks dannelse mellem en krystal af aktiverede søjle[5]arener og en poly(ethylenoxid) smelte. Kredit:Kanazawa University Forskere ved Kanazawa University rapporterer i Natur
- To forbindelser, der har den samme molekylære formel, men forskellige strukturelle formler er?
- En biologisk løsning på kulstofopsamling og genanvendelse?
- Hvor mange ML i 56CL?
- Hvad er fordele og ulemper ved kloningsplanter?
- Hvor tror du, vi mennesker får energi?
- Computersimulering forklarer, hvorfor zebraer har striber


