Afbalanceret kemisk ligning for jernrustning:Fra jern til jern(III)hydroxid
Af Chris Deziel – Opdateret 30. august 2022
Rust, den velkendte rødlige korrosion af jern, er ikke kun et terrestrisk fænomen. Det er blevet identificeret på Mars, hvor jernoxider giver planeten dens karakteristiske nuance og antyder en vådere, iltrig fortid.
Hvorfor rust er relevant for planetarisk videnskab
Tilstedeværelsen af rust på Mars-overfladen tyder på, at flydende vand engang fandtes i overflod, og at atmosfæren indeholdt nok ilt til at drive oxidationen af jern. At forstå den underliggende kemi hjælper videnskabsmænd med at fortolke Mars geologi og vurdere planetens beboelighed.
Kemi ved rust
Rust dannes, når jern reagerer med ilt i nærvær af vand. Den overordnede reaktion kan skrives som:
4Fe + 3O₂ + 6H₂O → 4Fe(OH)₃
Denne afbalancerede ligning opsummerer flertrinsprocessen, der begynder med opløsningen af fast jern og slutter med dannelsen af hydreret jern(III)hydroxid, som dehydrerer til den velkendte Fe₂O₃·H₂O.
Trin 1 – Oxidation af fast jern
Når jern udsættes for et vandigt miljø, undergår det oxidation:
Fe(r) → Fe²⁺(aq) + 2e⁻
De frigjorte elektroner reducerer opløst ilt i nærvær af hydrogenioner til dannelse af vand:
4e⁻ + 4H+(aq) + O₂(aq) → 2H2O(l)
Trin 2 – Dannelse af hydreret jernoxid
Hydroxidioner produceret i det første trin kombineres med Fe²⁺ for at producere grønt jern(II)hydroxid:
Fe²⁺(aq) + 2OH⁻(aq) → Fe(OH)₂(s)
Samtidig oxideres Fe2+ yderligere til Fe3+:
4Fe²⁺(aq) + 4H⁺(aq) + O₂(aq) → 4Fe³⁺(aq) + 2H₂O(l)
Endelig reagerer Fe³⁺ med hydroxid og danner jern(III)hydroxid:
Fe³⁺(aq) + 3OH⁻(aq) → Fe(OH)₃(s)
Ved dehydrering giver Fe(OH)3 rustmineralet Fe2O3·H2O.
Skrivning af den balancerede ligning
For at afbalancere den overordnede reaktion, tæl atomer på hver side og juster koefficienter. Med udgangspunkt i reaktanterne Fe, O₂ og H₂O og produktet Fe(OH)3 er den balancerede form:
4Fe + 3O₂ + 6H₂O → 4Fe(OH)₃
Denne ligning viser, at der kræves fire jernatomer, tre iltmolekyler og seks vandmolekyler for at producere fire enheder jern(III)hydroxid.
Konklusion
Rust er en klar indikator for tidligere miljøforhold på Jorden og, spændende nok, på Mars. Ved at forstå dens afbalancerede kemiske vej kan både kemikere og planetforskere bedre fortolke tilstedeværelsen af jernoxider i forskellige omgivelser.
 Varme artikler
Varme artikler
-
 Et meget følsomt SERS-substrat til gassensingSERS-sensoren. Kredit:SIBET Sporgassensing er afgørende for overvågning af miljøforurening og detektering af flygtige organiske forbindelser frigivet fra den menneskelige krop. Som et kraftfuldt a
Et meget følsomt SERS-substrat til gassensingSERS-sensoren. Kredit:SIBET Sporgassensing er afgørende for overvågning af miljøforurening og detektering af flygtige organiske forbindelser frigivet fra den menneskelige krop. Som et kraftfuldt a -
 Hvad gør den dødbringende pufferfish så lifligForskere har identificeret de vigtigste forbindelser, der er ansvarlige for smagen af pufferfish ( Takifugu obscurus ). Kredit:Yuan Liu Nogle mennesker overvejer pufferfish, også kendt som fug
Hvad gør den dødbringende pufferfish så lifligForskere har identificeret de vigtigste forbindelser, der er ansvarlige for smagen af pufferfish ( Takifugu obscurus ). Kredit:Yuan Liu Nogle mennesker overvejer pufferfish, også kendt som fug -
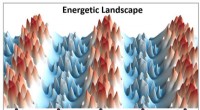 En fundamentalt ny tilgang til elektrostatisk design af materialer3D-vision af det manipulerede energilandskab inden for tredimensionelt bulkmateriale. Kredit:TU Graz Forskere ved Institute of Solid State Physics kortlægger en radikalt ny tilgang til design af o
En fundamentalt ny tilgang til elektrostatisk design af materialer3D-vision af det manipulerede energilandskab inden for tredimensionelt bulkmateriale. Kredit:TU Graz Forskere ved Institute of Solid State Physics kortlægger en radikalt ny tilgang til design af o -
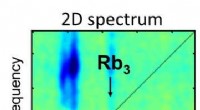 Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk
Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk
- Hvorfor stråler al den energi, der er optaget af Jorden, tilbage i rummet om natten?
- Det handler i sidste ende om at forudsige alt - teori kunne være et kort i jagten på kvantemateria…
- Forskere nærmer sig 12 milliarder år gamle signaler fra slutningen af universets mørke tidsalde…
- Carbonlagring i høstede træprodukter
- Nucleation en velsignelse for bæredygtig nanofremstilling
- Hvad beskriver bedst en gas?


