4 gennemprøvede strategier til at fremskynde kemiske reaktioner
Af Vaibhav Rakesh – Opdateret 30. august 2022
Totojang/iStock/GettyImages
En kemisk reaktion er drevet af kollisioner mellem reaktantmolekyler. En reaktions hastighed kan øges ved at manipulere flere nøglefaktorer, der påvirker kollisionsfrekvens og energi. Nedenfor er fire evidensbaserede tilgange, der pålideligt øger reaktionshastigheden.
1. Brug en Catalyst
En katalysator er et stof, der sænker aktiveringsenergien af en reaktion uden at blive forbrugt eller ændre slutprodukterne. Fordi det skaber en alternativ, lavere energi-vej, øger katalysatorer dramatisk antallet af produktive kollisioner. For eksempel begynder nedbrydningen af kaliumchlorat (KClO₃) ved 392°F, når mangandioxid (MnO₂) er til stede, hvorimod den samme reaktion uden en katalysator først starter ved 715°F.
2. Øg temperaturen
En hævning af temperaturen injicerer kinetisk energi i reaktantmolekyler, hvilket får dem til at bevæge sig hurtigere og kollidere oftere. Forholdet er ofte lineært op til et punkt, hvorefter sidereaktioner eller nedbrydning kan dominere. En almindelig illustration er, at sukker opløses hurtigere i varmt vand end i koldt vand, da forhøjet temperatur accelererer diffusions- og kollisionsprocesserne.
3. Koncentrer reaktanterne
Kollisionsteori forudsiger, at højere reaktantkoncentration øger sandsynligheden for kollisioner. For gasser kan dette opnås ved at hæve trykket og derved komprimere molekyler til et mindre volumen. I væsker eller faste stoffer øger blot tilsætning af mere reaktantmasse den samlede kollisionshastighed og fremskynder reaktionen.
4. Forøg overfladearealet
Mere eksponeret overfladeareal betyder, at flere molekyler er tilgængelige for kontakt på ethvert givet tidspunkt. Konvertering af reaktanter til pulveriserede eller findelte former maksimerer denne effekt. Pulveriseret sukker opløses hurtigere end en sukkerterning, og forbrændingen er langt hurtigere, når brændstof er i fine partikelform.
Disse strategier – katalysatorer, temperatur, koncentration og overfladeareal – er hjørnestenene i kemisk kinetik og anvendes rutinemæssigt i industrielle processer, laboratorier og daglige applikationer til at kontrollere reaktionshastigheden.
 Varme artikler
Varme artikler
-
 Probe skinner lys på overaktive immunceller for at hjælpe med at opdage, behandle visse kræftform…Purdue University-forskere har udviklet en ny sonde til at overvåge og mærke immunproteasom-udtrykkende celler. Kredit:Purdue University En frustration for læger og patienter, der beskæftiger sig
Probe skinner lys på overaktive immunceller for at hjælpe med at opdage, behandle visse kræftform…Purdue University-forskere har udviklet en ny sonde til at overvåge og mærke immunproteasom-udtrykkende celler. Kredit:Purdue University En frustration for læger og patienter, der beskæftiger sig -
 Hunde kan opdage spor af benzin ned til en milliardtedel af en teskefuldEza venter på sin handler, Jeff Lunder, at påbegynde en ransagning af en boligbrand for at kontrollere, om der er tegn på antændelig væske. Fotokredit:Joe Towers Kredit:Joe Towers Trænede hunde ka
Hunde kan opdage spor af benzin ned til en milliardtedel af en teskefuldEza venter på sin handler, Jeff Lunder, at påbegynde en ransagning af en boligbrand for at kontrollere, om der er tegn på antændelig væske. Fotokredit:Joe Towers Kredit:Joe Towers Trænede hunde ka -
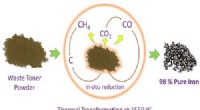 Træk jern ud af spildprintertonerKredit:American Chemical Society En skønne dag, rester af toner i kasserede printerpatroner kan have et nyt liv som bro eller bygningsdele i stedet for som skraldespand, spilde væk på lossepladser
Træk jern ud af spildprintertonerKredit:American Chemical Society En skønne dag, rester af toner i kasserede printerpatroner kan have et nyt liv som bro eller bygningsdele i stedet for som skraldespand, spilde væk på lossepladser -
 Nulemissionsdieselforbrænding ved hjælp af et ikke-ligevægtsplasma-assisteret MnO2-filterAktiverede kemiske arter (O 3 , OH-radikaler osv.) dannes ved at inducere et atmosfærisk tryk ikke-ligevægtsplasma. Disse arter fremmer afsvovlings- og denitreringsreaktioner med MnO 2 . I denne a
Nulemissionsdieselforbrænding ved hjælp af et ikke-ligevægtsplasma-assisteret MnO2-filterAktiverede kemiske arter (O 3 , OH-radikaler osv.) dannes ved at inducere et atmosfærisk tryk ikke-ligevægtsplasma. Disse arter fremmer afsvovlings- og denitreringsreaktioner med MnO 2 . I denne a
- Hvorfor er ældre bjerge og vulkaner mindre end yngre?
- At have et ur i dit brusebad kan være med til at reducere vandforbruget
- Hvorfor vidste gamle astronauter om Venus?
- Hvilket system regulerer metabolismens vækst og funktioner af seksuelle organer?
- Ny undersøgelse viser, at nikkelgrafen kan tunes til optimal brudstyrke
- Stabling og vridning af grafen låser op for en sjælden form for magnetisme


