Hvad bestemmer et atoms kemiske adfærd? Elektronkonfigurationens rolle
Af Veronica Mitchell Opdateret 30. august 2022
statu-nascendi/iStock/GettyImages
TL;DR
Atomer reagerer ved at vinde, miste eller dele elektroner. Deres reaktivitet afhænger af, hvor let de kan ændre deres ydre elektronskal.
Atomstruktur
Atomer er bygget af tre subatomære partikler:protoner, neutroner og elektroner. Atomnummeret – antallet af protoner – identificerer grundstoffet; for eksempel er ethvert atom med seks protoner kulstof. Neutrale atomer opretholder lige mange positivt ladede protoner og negativt ladede elektroner. Elektroner kredser om kernen i energiniveauer eller skaller, der er arrangeret tættest på længst fra kernen. Hver skal kan kun rumme et begrænset antal elektroner, så de yderste elektroner - kendt som valenselektroner - er afgørende for at bestemme kemisk adfærd.
Valence Electron Configuration
Fordi antallet af elektroner er lig med antallet af protoner, har de fleste atomer en delvist fyldt ydre skal. Når atomer møder andre arter, har de en tendens til at opnå en fuld valensskal, enten ved at miste elektroner, få elektroner eller dele elektroner gennem kovalente bindinger. Denne drift mod en stabil konfiguration gør det muligt for kemikere at forudsige et atoms reaktivitet ved at undersøge dets elektronkonfiguration. Ædelgasser som neon og argon er inerte, fordi de allerede har en komplet ydre skal, og de deltager sjældent i reaktioner, medmindre de udsættes for ekstreme forhold.
Det periodiske system
Det periodiske system arrangerer grundstoffer, så atomer med lignende egenskaber optræder i samme kolonne eller gruppe. Gruppe 1-elementer – natrium, kalium og andre – indeholder hver en enkelt valenselektron, der er svagt fastholdt af kernen. Følgelig mister disse atomer let den elektron, hvilket gør dem meget reaktive. I modsætning hertil har gruppe 17-elementer ét tomt sted i deres ydre skal; de er ivrige efter at acceptere en elektron, hvilket forklarer deres høje elektronegativitet og reaktivitet.
Ioniseringsenergi
Ioniseringsenergi (I.E.) er den energi, der kræves for at fjerne en elektron fra et atom. En lav første ioniseringsenergi indikerer, at et atom nemt kan afgive sin ydre elektron. Ioniseringsenergier måles for successiv fjernelse af elektroner:den første I.E. fjerner den yderste elektron, den anden fjerner den næste, og så videre. For eksempel har calcium (Gruppe 2) en første I.E. på 590 kJmol⁻¹ og en anden I.E. på 1145 kJmol⁻¹, men en markant højere tredjedel I.E. på 4912 kJmol⁻¹. Disse værdier tyder på, at calcium typisk mister sine to første elektroner under kemiske reaktioner.
Elektronaffinitet
Elektronaffinitet (Eₐ) måler, hvor let et atom accepterer en elektron. En meget negativ elektronaffinitet indikerer en stærk tendens til at få en elektron. Fluor, det mest reaktive grundstof, har en elektronaffinitet på –328 kJmol⁻¹, hvilket gør det usædvanligt ivrig efter at modtage elektroner. Ligesom ioniseringsenergier afslører successive elektronaffiniteter, hvordan et element vil opføre sig, når det interagerer med andre arter.
 Varme artikler
Varme artikler
-
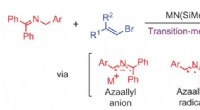 Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk
Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk -
 Hvordan molekylestørrelse former væskeviskositetFascinadora/iStock/GettyImages Viskositet kvantificerer en væskes modstand mod strømning. Blandt mange påvirkningsfaktorer spiller størrelsen af dets konstituerende molekyler en central rolle. Når
Hvordan molekylestørrelse former væskeviskositetFascinadora/iStock/GettyImages Viskositet kvantificerer en væskes modstand mod strømning. Blandt mange påvirkningsfaktorer spiller størrelsen af dets konstituerende molekyler en central rolle. Når -
 Beregningsanalyse afslører den komplekse adfærd af en polymerFigur 1:Konventionelle plastmaterialer som f.eks. Disse plasticchips fra genanvendte vandflasker er vanskelige at nedbryde i deres monomer byggesten. Nu, RIKEN -forskere har afsløret den komplekse dep
Beregningsanalyse afslører den komplekse adfærd af en polymerFigur 1:Konventionelle plastmaterialer som f.eks. Disse plasticchips fra genanvendte vandflasker er vanskelige at nedbryde i deres monomer byggesten. Nu, RIKEN -forskere har afsløret den komplekse dep -
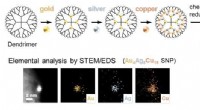 Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T
Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T
- Hvad kan der ses af jorden, fordi de reflekterer lys et objekt?
- Hvordan er oceanisk skorpe og kontinentale ens?
- Computermodel hjælper med at give mening i menneskets hukommelse
- 9 stater sagsøger EPA for fuldstændig dispensation, da nation bekæmper pandemi
- Et flygtigt øjeblik i tiden
- Hvordan teknologiske fremskridt former miljøet:risici, ressourceforbrug og bortskaffelse


