Forståelse af forbrændingsreaktioner:Hvordan ild omdanner brændstof til energi
En forbrændingsreaktion, ofte forkortet RXN, er den kemiske proces, hvor et brændbart stof reagerer med ilt og frigiver varme og lys.
Mens mange reaktioner producerer varme, deler ægte forbrændingsreaktioner specifikke egenskaber:de involverer oxygen, producerer energi og resulterer typisk i kuldioxid og vanddamp, når kulbrinter er involveret.
TL;DR
Forbrænding =brændstof + ilt → varme + lys. Kulbrinter (træ, benzin, propan) brænder til CO₂ og H₂O. Andre forbrændinger, såsom magnesiumforbrænding, genererer MgO uden CO₂.
Hvordan forbrænding opstår
For at forbrændingen kan starte, er tre elementer afgørende:et brændstof, ilt og en antændelseskilde. Mens nogle materialer antændes spontant, kræver de fleste en ekstern gnist eller flamme for at bryde deres molekylære bindinger.
Når reaktionen begynder, er den producerede varme tilstrækkelig til at opretholde processen, hvilket gør brændstoffet til en kontinuerlig flamme, indtil det reaktive materiale er opbrugt. Urenheder i brændstoffet fremstår som aske, mens fugt kan slukke flammen ved at absorbere varme for at fordampe vand.
Typisk forbrændingseksempel:Metan
Naturgasovne er afhængige af metan (CH₄) forbrænding. Reaktionen forløber som:
CH4 + 2O2 → CO2 + 2H2O
Pilotlyset eller gnisten leverer den indledende energi, hvorefter den eksoterme reaktion genererer varme og lys til madlavning.
Ikke-kulbrinteforbrænding:Magnesium
Magnesium brænder i luften og danner magnesiumoxid (MgO). Dens forbrændingsligning er:
2Mg + O2 → 2MgO
I modsætning til kulbrintebrande udsender denne reaktion ingen CO₂ eller H₂O, men producerer intens varme og en klar hvid flamme, hvilket illustrerer, at forbrænding ikke behøver at producere traditionelle brandprodukter.
Vigtige ting
Forbrænding er en kontrolleret, eksoterm reaktion mellem brændstof og ilt, der producerer varme og lys. At forstå dens mekanik hjælper med at designe sikrere motorer, effektive varmeapparater og bedre brandsikkerhedsprotokoller.
Lær mere om forbrændingskemi her .
 Varme artikler
Varme artikler
-
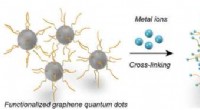 Kvantepunkter holder atomer i afstand for at øge katalysenIngeniører fra Rice University har ledet udviklingen af en proces, der bruger funktionaliserede grafenkvantepunkter til at fange overgangsmetaller til højere metalbelastning enkeltatomskatalyse. Kre
Kvantepunkter holder atomer i afstand for at øge katalysenIngeniører fra Rice University har ledet udviklingen af en proces, der bruger funktionaliserede grafenkvantepunkter til at fange overgangsmetaller til højere metalbelastning enkeltatomskatalyse. Kre -
 Inspirerer folk til at træffe bedre livsstilsvalg – gennem isotoperForskerne Amrita Rhoads og Gwyneth Gordon måler isotopforhold i en hårprøve for at vurdere, hvad deltagerne typisk spiste. Kredit:ASU Fitnessmål er typisk på forkant med nytårsforsæt for mange ame
Inspirerer folk til at træffe bedre livsstilsvalg – gennem isotoperForskerne Amrita Rhoads og Gwyneth Gordon måler isotopforhold i en hårprøve for at vurdere, hvad deltagerne typisk spiste. Kredit:ASU Fitnessmål er typisk på forkant med nytårsforsæt for mange ame -
 For at opsnuse kriminalitet og forsvundne personer, videnskaben støtter bloddetektionshundeHunde kan pålideligt opsnuse menneskeblod, selv efter to års miljøforringelse. Kredit:Jason Korbol/shutterstock Det er svært at overveje tragedien ved at miste en elsket en og aldrig vide, hvad de
For at opsnuse kriminalitet og forsvundne personer, videnskaben støtter bloddetektionshundeHunde kan pålideligt opsnuse menneskeblod, selv efter to års miljøforringelse. Kredit:Jason Korbol/shutterstock Det er svært at overveje tragedien ved at miste en elsket en og aldrig vide, hvad de -
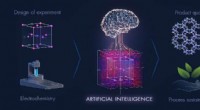 Maskinlæring kunne lære os, hvordan man gør fremstilling af materialer renere og mere bæredygtigMaskinlæring og design af eksperimenter kan kombineres for at identificere den mest bæredygtige metode til udvikling af avancerede materialer. Kredit:020 KAUST; Xavier Pita Kemi computeralgoritme
Maskinlæring kunne lære os, hvordan man gør fremstilling af materialer renere og mere bæredygtigMaskinlæring og design af eksperimenter kan kombineres for at identificere den mest bæredygtige metode til udvikling af avancerede materialer. Kredit:020 KAUST; Xavier Pita Kemi computeralgoritme
- Lav en kerne mad til planter?
- Efterhånden som vegansk aktivisme vokser, politikere har til formål at beskytte agri-business, res…
- Bærer kortbølgelængde lys mere energi eller mindre end langbølgelængde lys?
- Ingen forudsætninger nødvendige for at simulere petroleumsreservoirer
- Hvad er nogle vigtige spørgsmål at stille om solsystemet?
- Strømgenererende materiale til organisk solcelle


