Biologiske nøglebuffere, der opretholder homeostase
Af David Stewart | Opdateret 30. august 2022
Motortion/iStock/GettyImages
En buffer er et kemisk stof, der stabiliserer pH i en opløsning, selv når der tilsættes syrer eller baser. I levende systemer er buffering afgørende for at opretholde et stabilt indre miljø - homeostase. Små molekyler såsom bikarbonat og fosfat, såvel som makromolekyler som hæmoglobin og proteiner, giver alle denne bufferkapacitet.
Bikarbonatbuffer
Bicarbonatbuffersystemet regulerer blodets pH gennem en dynamisk ligevægt mellem kulsyre (H2CO3) og bikarbonationer (HCO3⁻). Når blodet bliver for surt, omdanner bufferen overskydende brintioner til kuldioxid, som lungerne derefter udstøder. Omvendt udskilles bikarbonat under alkalose i urinen, hvilket genopretter neutral pH.
Fosfatbuffer
I celler giver fosfatbufferen - omfattende hydrogenphosphat (HPO₄²⁻) og dihydrogenphosphat (H₂PO₄⁻) - en stærkere bufferkapacitet end bicarbonatsystemet. Det neutraliserer overskydende hydrogenioner ved at danne de mindre reaktive fosfattyper, og under alkaliske forhold accepterer det hydroxidioner, hvorved det intracellulære miljø vender tilbage til neutralitet.
Proteinbuffer
Proteiner, bygget af aminosyrer forbundet med peptidbindinger, har sidekæder, der kan donere eller acceptere protoner. Ved fysiologisk pH eksisterer carboxylgrupper som negativt ladede carboxylationer (COO⁻), mens aminogrupper protoneres som NH3+. Under sure forhold fanger carboxylater protoner for at danne COOH, og under alkaliske forhold frigiver NH3⁺ protoner og bliver til NH₂ – begge handlinger dæmper pH-udsving.
Hæmoglobinbuffer
Hæmoglobin, det iltbærende pigment i røde blodlegemer, puffer også vævets pH. Dens globinunderenheder kan binde protoner, mens hæmjernet binder ilt. Under træning optages overskydende protoner af hæmoglobin, som samtidig frigiver ilt og derved mindsker syreopbygningen i musklerne.
 Varme artikler
Varme artikler
-
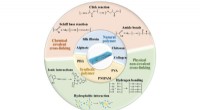 Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse
Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse -
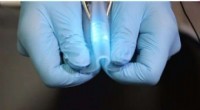 Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi
Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi -
 Dens elementære:Ultra-spordetektor tester guldrenhedKhadouja Harouaka (siddende) og Isaac Arnquist forbereder prøver i et ultrarent laboratorium, hvilket er nødvendigt for at sikre nøjagtige massespektrometrimålinger. Kredit:Andrea Starr | Pacific Nort
Dens elementære:Ultra-spordetektor tester guldrenhedKhadouja Harouaka (siddende) og Isaac Arnquist forbereder prøver i et ultrarent laboratorium, hvilket er nødvendigt for at sikre nøjagtige massespektrometrimålinger. Kredit:Andrea Starr | Pacific Nort -
 Beregning af Parts-Per-Billion (PPB) i vandige opløsningerAf Jack Brubaker, Opdateret Aug302022 obeyleesin/iStock/GettyImages I kemi udtrykkes koncentrationer i en række enheder. En opløsning består af et opløst stof - forbindelsen til stede i den mindre m
Beregning af Parts-Per-Billion (PPB) i vandige opløsningerAf Jack Brubaker, Opdateret Aug302022 obeyleesin/iStock/GettyImages I kemi udtrykkes koncentrationer i en række enheder. En opløsning består af et opløst stof - forbindelsen til stede i den mindre m
- Er smeltende voks en fast væske eller gas?
- Hvad kan det være et problem med at bruge energi fra vind og sol?
- Sådan kontrolleres om en diode er dårlig
- Forskere skal udforske nye steder i Puerto Rico, USVI farvande
- Når kun en sliver del af måneoverfladen lyser, hvad den kaldte?
- Hvem har brug for transistorer? HP-forskere skaber nyt computergennembrud i molekylær skala


