Beregning af Parts-Per-Billion (PPB) i vandige opløsninger
Af Jack Brubaker, Opdateret Aug302022
obeyleesin/iStock/GettyImages
I kemi udtrykkes koncentrationer i en række enheder. En opløsning består af et opløst stof - forbindelsen til stede i den mindre mængde - og et opløsningsmiddel. En af de mest almindelige måder at udtrykke koncentration på er masseprocent (også kendt som vægtprocent), beregnet som (masse af opløst stof ÷ masse af opløsning)×100. Når opløsninger er ekstremt fortyndede, bliver masseprocentværdien meget lille, så kemikere skalerer ofte forholdet med 10⁹ i stedet for 100, hvilket producerer dele pr. milliard (ppb).
Trin 1 – Bestem masser
Identificer først massen af det opløste stof og massen af hele opløsningen. For en vandbaseret opløsning er 1mL væske lig med 1g, så 1L vand er lig med 1000g. For eksempel giver opløsning af 0,005 g natriumchlorid (NaCl) i vand og derefter fortynding til et slutvolumen på 1,0 L 0,005 g opløst stof i 1000 g opløsning.
Trin 2 – Beregn masseforholdet
Divider den opløste masse med opløsningens masse:0,005g ÷ 1000g=5×10⁻⁶. Dette forhold repræsenterer koncentrationen i fraktioneret.
Trin 3 – Konverter til PPB
Multiplicer forholdet med 1000000000 for at udtrykke det som dele pr. milliard:5×10⁻⁶×10⁹=5000ppb.
TL;DR
For vandige opløsninger kan ppb-beregningen forenkles til mikrogram opløst stof pr. liter opløsning. Konverter gram til mikrogram ved at gange med 1000000.
 Varme artikler
Varme artikler
-
 Det tosprogede molekyle forbinder to grundlæggende koder for livetDet nye molekyle rummer potentialet for forskellige biomedicinske anvendelser, siger Emory -kemiker Jennifer Heemstra (til højre), seniorforfatter af papiret. Hun vises i sit laboratorium med kandidat
Det tosprogede molekyle forbinder to grundlæggende koder for livetDet nye molekyle rummer potentialet for forskellige biomedicinske anvendelser, siger Emory -kemiker Jennifer Heemstra (til højre), seniorforfatter af papiret. Hun vises i sit laboratorium med kandidat -
 Ser nærmere på elektrificerende kemiSpektroelektrokemisk laboratorium ved Institut for Kemi og Farmaci ved Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU). Fra venstre:Prof. Dr. Jörg Libuda, Dr. Olaf Brummel, som holder en infra
Ser nærmere på elektrificerende kemiSpektroelektrokemisk laboratorium ved Institut for Kemi og Farmaci ved Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU). Fra venstre:Prof. Dr. Jörg Libuda, Dr. Olaf Brummel, som holder en infra -
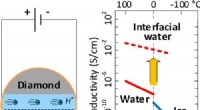 Forskere måler elektrisk ledningsevne af rent grænsefladevandGrafisk abstrakt. Kredit: Journal of Physical Chemistry Letters Skoltech-forskere i samarbejde med forskere fra universitetet i Stuttgart, Karlsruhe Institute of Technology og Russian Quantum Cen
Forskere måler elektrisk ledningsevne af rent grænsefladevandGrafisk abstrakt. Kredit: Journal of Physical Chemistry Letters Skoltech-forskere i samarbejde med forskere fra universitetet i Stuttgart, Karlsruhe Institute of Technology og Russian Quantum Cen -
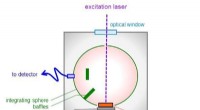 Forskere forbedrer metoden til at sondere halvledende krystaller med lys for at opdage defekter og u…Prøven placeres uden for den integrerende kugle og på en aluminiumsplade forbundet til en køleanordning. Kredit:Tohoku University Forskere fra Tohoku University har forbedret en metode til at sond
Forskere forbedrer metoden til at sondere halvledende krystaller med lys for at opdage defekter og u…Prøven placeres uden for den integrerende kugle og på en aluminiumsplade forbundet til en køleanordning. Kredit:Tohoku University Forskere fra Tohoku University har forbedret en metode til at sond
- Hvad sker der, når to objekter, der har den samme temperatur touch?
- På Jesu fødested, en app er født for at lette folkemængderne
- Hårde arter af koraller kan blive mobile og lægge grunden til nye rev i ellers ugæstfrie områder…
- Hvorfor Anthurium forårsager negativ energi?
- Native Plants & Animals of China
- Exoplaneter vil have brug for både kontinenter og oceaner for at danne komplekst liv


