Sådan beregnes bikarbonatkoncentration i vandprøver
Af John Brennan | Opdateret 30. august 2022
Når kuldioxid opløses i vand, danner det kulsyre (H₂CO₃). Denne syre kan dissociere for at give bicarbonat (HCO3⁻) eller carbonat (CO32⁻). Calciumioner i vandet vil reagere med disse arter for at producere enten opløseligt calciumbicarbonat eller uopløseligt calciumcarbonat. Til miljø- og vandkvalitetstestning er beregning af bicarbonatkoncentrationen ud fra total alkalitet og pH et almindeligt krav.
Trin 1:Konverter total alkalinitet til molaritet
Total alkalinitet udtrykkes sædvanligvis i milligram pr. liter CaCO3. Divider værdien med 100 000 gmol⁻¹ for at opnå mol pr. liter (molaritet). Dette trin giver den basislinjekoncentration, der vil blive forfinet i de næste trin.
Trin 2:Erstat karbonatligningen med alkalinitetsudtrykket
Den generelle alkalinitetsformel er:
2×Total alkalinitet = [HCO₃⁻] + 2[CO₃²⁻] + [OH⁻]
Med carbonatkoncentrationen udtrykt som [CO₃²⁻] = (K₂ [HCO₃⁻])/[H⁺] , hvor K₂ = 5,6×10⁻¹¹, bliver ligningen:
2×Total alkalinitet = [HCO₃⁻] + 2×(K₂ [HCO₃⁻]/[H⁺]) + [OH⁻]
Trin 3:Løs for [HCO₃⁻]
Brug af forholdet [H⁺] = 10^(−pH) og hydroxidkoncentrationen [OH⁻] = 10^(−14 + pH) , er den algebraiske løsning:
[HCO₃⁻] = (2×Total Alkalinitet – 10^(−14 + pH)) / (1 + 2K₂ × 10^(pH))
Trin 4:Beregn bikarbonatkoncentration
Indsæt molariteten af CaCO₃ opnået i trin 1 i formlen ovenfor. Resultatet er bicarbonatkoncentrationen i mol pr. liter.
Hvad du skal bruge
- Samlet alkalinitet af prøven
- pH i prøven
- Blyant og papir
- Lommeregner
- Anden dissociationskonstant for kulsyre (K₂ = 5,6×10⁻¹¹)
Vigtig bemærkning
Afledningen antager, at calcium- og carbonatarter dominerer alkaliniteten. Hvis andre alkaliske komponenter - såsom ammoniak - er til stede, er en mere sofistikeret model påkrævet. Se det første link under afsnittet "Referencer" for yderligere vejledning.
Sidste artikelBeregning af Parts-Per-Billion (PPB) i vandige opløsninger
Næste artikelSådan tælles atomer nøjagtigt i kemiske formler
 Varme artikler
Varme artikler
-
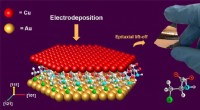 Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis
Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis -
 Skaber et ikke-giftigt alternativ til farvet røgKredit:imago images / Shotshop Farvet røg bliver i stigende grad brugt som et skueelement i et bredt spektrum af offentlige arrangementer. Imidlertid, de kemikalier, der anvendes til dette formål,
Skaber et ikke-giftigt alternativ til farvet røgKredit:imago images / Shotshop Farvet røg bliver i stigende grad brugt som et skueelement i et bredt spektrum af offentlige arrangementer. Imidlertid, de kemikalier, der anvendes til dette formål, -
 Traditionelle hemmeligheder til at holde sig kølig – undersøgelse af Okinawan-tekstilerForstørrede billeder af vaskulære bundter efter traditionel digumering i Naha-u, den yderste del af bananplantens bladskede, der bruges til at lave Basho-fu. Kredit:Journal of Fiber Science and Techno
Traditionelle hemmeligheder til at holde sig kølig – undersøgelse af Okinawan-tekstilerForstørrede billeder af vaskulære bundter efter traditionel digumering i Naha-u, den yderste del af bananplantens bladskede, der bruges til at lave Basho-fu. Kredit:Journal of Fiber Science and Techno -
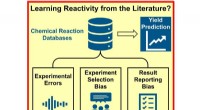 Hvor tydeligere rapportering af negative eksperimentelle resultater ville forbedre reaktionsplanlæg…Kredit:Angewandte Chemie Databaser indeholdende enorme mængder eksperimentelle data er tilgængelige for forskere på tværs af en lang række kemiske discipliner. Et team af forskere har imidlertid op
Hvor tydeligere rapportering af negative eksperimentelle resultater ville forbedre reaktionsplanlæg…Kredit:Angewandte Chemie Databaser indeholdende enorme mængder eksperimentelle data er tilgængelige for forskere på tværs af en lang række kemiske discipliner. Et team af forskere har imidlertid op


