Beregning af molprocent:en trin-for-trin guide til nøjagtig blandingsanalyse
Af Jack Brubaker
Opdateret 30. august 2022
Rawpixel/iStock/GettyImages
I fysisk kemi fortæller molfraktionen - eller molprocenten - af en komponent dig, hvor mange mol af det stof der findes i forhold til det samlede antal mol i en blanding. En muldvarp er lig med 6,022 x 10 23 atomer eller molekyler. For at finde molprocenten skal du først bestemme mol for hver komponent ved at dividere dens masse med dens molekylvægt, derefter dividere dette tal med summen af alle mol og gange med 100.
1. Bestem masse
Optag massen af hver art i blandingen. Hvis du allerede har forberedt opløsningen, skal massen være opført i protokollen. Hvis du opretter blandingen, skal du notere gram af hver forbindelse. For eksempel en opløsning af 10 g NaCl med 100 g H2 O. Hvis du arbejder i ounces, skal du konvertere til gram med en pålidelig online lommeregner.
2. Beregn molekylvægt
Beregn formelvægten for hver komponent ved at gange antallet af atomer af hvert element med dets atomvægt (fra et pålideligt periodisk system, såsom NIST-databasen). Eksempel:NaCl =(1 × 22,99) + (1 × 35,45) =58,44 g/mol; H2 O =(2 × 1,01) + (1 × 16,00) =18,02 g/mol.
3. Opdel masse efter molekylvægt
Bestem mol af hvert stof:
- NaCl:10 g ÷ 58,44 g/mol =0,171 mol
- H2 O:100 g ÷ 18,02 g/mol =5,55 mol
4. Beregn molprocent
Find molprocenten af hver komponent:
- NaCl:(0,171 ÷ (0,171+5,55)) × 100 =2,99 %
- H2 O:(5,55 ÷ (5,55+0,171)) × 100 =97,01 %
Ting, der er nødvendige
- Plideligt periodisk system (f.eks. NIST eller IUPAC)
- Videnskabelig lommeregner eller regnearkssoftware
TL;DR (for lang; læste ikke)
For enhver blanding tilføjes molfraktioner til 100%. I vores eksempel på 10 g NaCl + 100 g vand er molprocenten af NaCl 2,99 % og den for vand 97,01 %.
Selvom udtrykkene "molekylvægt" og "formelvægt" teknisk adskiller kovalente fra ioniske forbindelser, er beregningsmetoden identisk i praksis.
 Varme artikler
Varme artikler
-
 Iridium-katalyseret hydrogenaddition, at give plante- og insektbaserede naturlige stofferKredit:Wiley Omkostningseffektiviteten af lægemiddelsyntese afhænger af en række faktorer, herunder mængden af affald produceret. Et team af forskere har nu opdaget en katalysator, der opnår u
Iridium-katalyseret hydrogenaddition, at give plante- og insektbaserede naturlige stofferKredit:Wiley Omkostningseffektiviteten af lægemiddelsyntese afhænger af en række faktorer, herunder mængden af affald produceret. Et team af forskere har nu opdaget en katalysator, der opnår u -
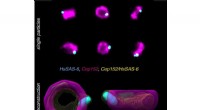 Superopløsningsmikroskopi bygger flerfarvet 3-D fra 2-DHumane centrioler mærket med antistoffer mod to proteiner (Cep152, HsSAS-6) og afbildet ved hjælp af superopløsningsmikroskopi. Fra mange individuelle partikler, der viser projektioner af centriolkomp
Superopløsningsmikroskopi bygger flerfarvet 3-D fra 2-DHumane centrioler mærket med antistoffer mod to proteiner (Cep152, HsSAS-6) og afbildet ved hjælp af superopløsningsmikroskopi. Fra mange individuelle partikler, der viser projektioner af centriolkomp -
 Forbedret katalysator kan oversætte til petrokemiske produktionsgevinsterKredit:CC0 Public Domain Aromatik er vigtige byggesten i polymerer, eller plastik, der dukker op som alt fra PET-flasker til vand til åndbare, rynkebestandigt polyestertøj. Disse petrokemikalier o
Forbedret katalysator kan oversætte til petrokemiske produktionsgevinsterKredit:CC0 Public Domain Aromatik er vigtige byggesten i polymerer, eller plastik, der dukker op som alt fra PET-flasker til vand til åndbare, rynkebestandigt polyestertøj. Disse petrokemikalier o -
 Brug af polymere membraner til at rense industrielle adskillelserZachary Smith er Joseph R Mares (1924) karriereudviklingsassistent professor i kemiteknik. Kredit:David Sella Der er snesevis af lovende teknologier under udvikling, der kan reducere energiforbrug
Brug af polymere membraner til at rense industrielle adskillelserZachary Smith er Joseph R Mares (1924) karriereudviklingsassistent professor i kemiteknik. Kredit:David Sella Der er snesevis af lovende teknologier under udvikling, der kan reducere energiforbrug
- Hvad er formlen for Platinumivoxid?
- Hvad er den vigtigste energikilde?
- Er det sandt, at et objekt, der bevæger sig med en konstant hastighed i lige sti, fortsat vil gøre…
- Hvad er hovedideen for vedvarende energiressourcer?
- Hvad vil der ske med et faldende objekt, hvis luftmodstanden, der virker på det, blev lige vægt af…
- Hvad sker der med sin hastighed, når man kaster en mønt opad, mens den er stigende acceleration?


