Forståelse af endergoniske reaktioner:energiinput, biologiske eksempler og sammenligning med eksergoniske processer
DuncanL/iStock/GettyImages
Endergoniske reaktioner er processer i fysisk kemi, der kræver et input af energi for at danne produkter, hvis frie energi overstiger reaktanternes. Når varme er den primære energibærer, kaldes reaktionen specifikt endoterm.
Endergoniske reaktioner
Disse ikke-spontane transformationer kræver ekstern energi. En klassisk biologisk illustration er fotosyntese, hvor planter absorberer sollys for at omdanne vand og kuldioxid til glukose - en forbindelse med højere fri energi end dens udgangsmaterialer. I kemiske termer er de bindinger, der dannes i en endergonisk reaktion, svagere end dem, der brydes, hvilket gør processen energetisk ugunstig uden en energikilde.
Et andet dagligdags eksempel er smeltningen af is:Når fast vand absorberer varme, går det over til flydende vand, en endoterm proces drevet af stigende temperaturer.
Eksergoniske reaktioner
Eksergoniske reaktioner er spontane; de frigiver energi til deres omgivelser og skaber bånd, der er stærkere end dem, der er brudt. Systemets frie energi falder. Almindelige eksempler omfatter syntesen af bordsalt fra natrium og klor og kemiluminescerende reaktioner, der udsender synligt lys. Når der frigives varme, er reaktionen også eksoterm.
Skelner Endergonic/Exergonic fra Endothermic/Exotermic
Mens "endergonisk" og "eksergonisk" refererer til nettoændringen i fri energi (ΔG), refererer "endotermisk" og "eksoterm" til entalpiændringen (ΔH). En reaktion kan således være endergonisk, men alligevel endoterm, eller eksergonisk, men alligevel eksoterm. For eksempel absorberer blanding af natriumcarbonat med citronsyre i vand varme (endotermisk) og er endergonisk. Omvendt frigiver en glow-stick-reaktion lys uden væsentlig varme og er eksergonisk, men ikke eksoterm.
I hverdagen kan du observere eksergoniske eksoterme reaktioner under tøjvask:tilsætning af vaskemiddel og vand giver en mild varmefornemmelse, hvilket indikerer energifrigivelse.
 Varme artikler
Varme artikler
-
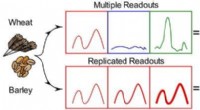 Et skridt i retning af følsom og hurtig glutenopdagelseKredit:American Chemical Society For mennesker med cøliaki og glutenfølsomhed, antallet af madmuligheder i butikkerne vokser. Men de nuværende test for gluten finder ikke alt stoffet i fødevarer,
Et skridt i retning af følsom og hurtig glutenopdagelseKredit:American Chemical Society For mennesker med cøliaki og glutenfølsomhed, antallet af madmuligheder i butikkerne vokser. Men de nuværende test for gluten finder ikke alt stoffet i fødevarer, -
 Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e
Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e -
 Syntetiske receptorer kan omkoble cellefunktioner og minimere bivirkningerKredit:CC0 Public Domain En af udfordringerne ved moderne farmakologi er specificitet. På trods af terapeutiske virkninger, medicin kan ofte have bivirkninger. Det biologiske grundlag for dette ha
Syntetiske receptorer kan omkoble cellefunktioner og minimere bivirkningerKredit:CC0 Public Domain En af udfordringerne ved moderne farmakologi er specificitet. På trods af terapeutiske virkninger, medicin kan ofte have bivirkninger. Det biologiske grundlag for dette ha -
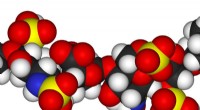 Den tid, der er nødvendig for at sekvensere nøglemolekyler, kan reduceres fra år til minutterEn nanopore og billedgenkendelsessoftware kan sekvensere en sulfateret glycosaminoglycan i realtid. Kredit:Rensselaer Polytekniske Institut Ved at bruge en nanopore, forskere har demonstreret pote
Den tid, der er nødvendig for at sekvensere nøglemolekyler, kan reduceres fra år til minutterEn nanopore og billedgenkendelsessoftware kan sekvensere en sulfateret glycosaminoglycan i realtid. Kredit:Rensselaer Polytekniske Institut Ved at bruge en nanopore, forskere har demonstreret pote
- Hvad er formålet med indlejring af elektrontransportkæde i membran en organisme?
- Rockefeller-forskere løser debat om, hvor mange bakterier, der bekæmper angribere
- Når du sammenligner hastigheden på to objekter, hvorfor skal du bruge de samme enheder?
- Nobelprisvindende arbejde er koncentreret i et mindretal af videnskabelige områder
- Er Petrel en rovdyr omnivore eller herbivore?
- Hvad er den energi, der bæres af hver enhed af en strøm, der kaldes?


