Sådan skriver du en kemisk formel - en praktisk vejledning
Af Karen G. Blaettler
Opdateret 30. august 2022
RapidEye/iStock/GettyImages
At forstå, hvordan man skriver en kemisk formel er afgørende for at kommunikere sammensætningen af enhver forbindelse. Med et klart greb om grundlæggende kemisk terminologi kan du trygt læse og skrive formler.
Nøgledefinitioner
Nøjagtigt sprog er rygraden i videnskaben. Nedenfor er essentielle udtryk, der vil hjælpe dig med at fortolke og skabe kemiske formler.
- Atom – Den mindste enhed af et grundstof, der omfatter en kerne (protoner og neutroner) og omgivende elektroner.
- Element – Et stof lavet af én type atom, identificeret med et unikt symbol på det periodiske system.
- Sammensat – Et stof dannet, når to eller flere forskellige atomer binder sig kemisk sammen.
- Molekyle – Den mindste enhed af en forbindelse, der bevarer sine kemiske egenskaber; molekyler er elektrisk neutrale.
- Ioner – Atomer eller grupper af atomer, der har fået eller mistet elektroner, hvilket resulterer i en netto positiv eller negativ ladning.
- Kemisk formel – En kortfattet repræsentation af et stofs sammensætning, der angiver typen og antallet af tilstedeværende atomer.
Elementsymboler
Hvert element har et symbol på et eller to bogstaver, der stammer fra dets engelske eller latinske navn (f.eks. Pb fra *plumbum* for bly). Når et symbol indeholder to bogstaver, skrives det første med stort, og det andet med små bogstaver.
Brug af tal i formler
Tal i en formel formidler specifik information:
- Tal før symbol angive, hvor mange atomer eller molekyler af den pågældende art er involveret (f.eks. 2O i C + 2O → CO₂).
- Abonnementer vis antallet af atomer direkte efter symbolet; fravær af et underskrift indebærer et atom (f.eks. har CO₂ et C og to O).
- Overskrift angive ladningen på en ion (f.eks. Mg²⁺, NO₃⁻).
- Når en polyatomisk ion optræder mere end én gang, omslutter parenteser ionen, og et underskrift følger efter den afsluttende parentes (f.eks. Mg(NO₃)₂).
Eksempel:I magnesiumnitrat er den balancerede ligningMg²⁺ + 2(NO₃)⁻ → Mg(NO₃)₂ , hvilket viser, at 2+ ladningen på Mg balancerer to 1-negative nitrationer for at producere en neutral forbindelse.
Latinske og græske præfikser
Præfikser hjælper med at identificere antallet af atomer eller ioner i en forbindelse:
- mono (1), bi/di (2), tri (3), tetra (4), penta (5), hexa (6), hepta (7)
For eksempel indeholder carbonmonoxid (CO) et C og et O, mens carbondioxid (CO₂) indeholder et C- og to O-atomer.
Almindelige polyatomiske ioner
- hydroxid – OH⁻
- carbonat – CO₃²⁻
- phosphat – PO₄³⁻
- nitrat – NO₃⁻
- sulfat – SO₄²⁻
Praktisk formelskrivning
Når du skriver en formel, skal du først anføre kationen (positiv ion) efterfulgt af anionen (negativ ion).
- Natriumchlorid (bordsalt):NaCl
- Carbontetrachlorid (opløsningsmiddel til kemisk rensning):CCl₄
- Natriumbicarbonat (bagepulver):Na₂CO₃ (bemærk:bikarbonationen er CO₃²⁻; formlen er Na₂CO₃)
- Dinitrogenheptachlorid :N2Cl7
- Ammoniumhydroxid (NH₃OH):NH₄OH – ammoniumionen (NH₄⁺) og hydroxidionen (OH⁻) kombineres og danner et neutralt molekyle.
Overgangsmetaller og romertal
Overgangsmetaller danner ofte ioner med flere ladninger. Ladningen er angivet i forbindelsens navn med et romertal:
- CuF2 er kobber(II)fluorid, fordi fluorid er 1⁻; derfor skal kobber være 2⁺.
- FeCl3 er jern(III)chlorid, der balancerer jern(III) (3⁺) med tre chloridioner (1⁻ hver).
- SnF₂ (stann(II)fluorid) og SnF₄ (stann(II)fluorid) illustrerer brugen af "stann(II)" for Sn²⁺ og "stannic" for Sn⁴⁺.
Forståelse af disse konventioner sikrer, at dine formler nøjagtigt afspejler den kemiske virkelighed af hver forbindelse.
 Varme artikler
Varme artikler
-
 Forskere opfinder metode til at skabe olefinerProf. Guangbin Dong (i midten) arbejder med medlemmer af hans laboratorium, postdoktorforsker Jun Zhu (tv) og kandidatstuderende Jianchun Wang. Kredit:Nancy Wong Olefiner er en af de molekyletyp
Forskere opfinder metode til at skabe olefinerProf. Guangbin Dong (i midten) arbejder med medlemmer af hans laboratorium, postdoktorforsker Jun Zhu (tv) og kandidatstuderende Jianchun Wang. Kredit:Nancy Wong Olefiner er en af de molekyletyp -
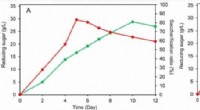 Ny konsolideret bio-saccharificeringsteknik til omdannelse af lignocellulose udvikletForsukring af forbehandlet hvedehalm under optimale eller regelmæssige forhold uden modifikation i både 100-ml anaerobe flasker (a) og en 10-L anaerob fermentor (b). Kredit:LIU Yajun En forskergru
Ny konsolideret bio-saccharificeringsteknik til omdannelse af lignocellulose udvikletForsukring af forbehandlet hvedehalm under optimale eller regelmæssige forhold uden modifikation i både 100-ml anaerobe flasker (a) og en 10-L anaerob fermentor (b). Kredit:LIU Yajun En forskergru -
 Forskere giver indsigt i letvægtsmateriale, der udvider sig med varmeKredit:Chong Min Koos gruppe ved Korea Institute of Science and Technology (KIST) Når det kommer til at tage plads uden at lægge for meget vægt, boblen kan ikke slås. Fordi de for det meste er luf
Forskere giver indsigt i letvægtsmateriale, der udvider sig med varmeKredit:Chong Min Koos gruppe ved Korea Institute of Science and Technology (KIST) Når det kommer til at tage plads uden at lægge for meget vægt, boblen kan ikke slås. Fordi de for det meste er luf -
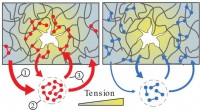 Udforsker, hvordan celler kan være stærke på det rigtige sted og på det rigtige tidspunktCatch bonds (rød) er svage i områder med lav spænding (1) og løsner derfor hurtigt (2). Disse ubundne binder igen på tilfældige steder i netværket, men binder kun tæt i højspændte områder (3), og fors
Udforsker, hvordan celler kan være stærke på det rigtige sted og på det rigtige tidspunktCatch bonds (rød) er svage i områder med lav spænding (1) og løsner derfor hurtigt (2). Disse ubundne binder igen på tilfældige steder i netværket, men binder kun tæt i højspændte områder (3), og fors
- Hvilke materialer kommer ind i chloroplasten, der bruges i lysafhængige reaktioner?
- Lavpris, fleksibel terahertz-strålingskilde til hurtig og ikke-invasiv screening
- Kvasikrystalklar:Materiale afslører en unik forskydende overfladestruktur under mikroskop
- Lykkeligning:Ny ligning afslører, hvordan andre menneskers formuer påvirker vores lykke
- Hvad laver linjer af Latitude measure?
- Hvorfor er gravitationsacklerationen af et objekt nær Jorden den samme?


