Sådan beregnes varme frigivet i eksoterme reaktioner
Af Claire Gillespie – Opdateret 30. august 2022
Nogle kemiske reaktioner frigiver varme, der overfører termisk energi til deres omgivelser. These are called exothermic reaktioner, hvor "exo" betyder ekstern og "termisk" henviser til varme.
Almindelige eksoterme processer omfatter forbrænding (brænding), oxidation (rustning) og neutralisering mellem syrer og baser. Daglige ting såsom håndvarmere og selvopvarmende kaffedåser er afhængige af disse reaktioner.
Hurtig reference
For at bestemme den frigivne varme skal du bruge formlen Q =m·c·ΔT :
- Q – heat energy transferred (J)
- m – mass of the liquid or substance (kg)
- c – specifik varmekapacitet (Jkg⁻¹°C⁻¹)
- ΔT – temperature change (°C)
Heat vs. Temperature
Temperaturen måler, hvor varmt en genstand er (°C eller °F). Varme er mængden af termisk energi et objekt indeholder, udtrykt i joule. Når varme tilføres, stiger temperaturen afhængigt af objektets masse, sammensætning og den tilførte energi.
Specific Heat Capacity
The specific heat capacity (c ) er den energi, der skal til for at hæve 1 kg af et stof med 1°C. Eksempler:
- Water:4,181 J kg⁻¹ °C⁻¹
- Oxygen:918 J kg⁻¹ °C⁻¹
- Lead:128 J kg⁻¹ °C⁻¹
Heat Energy Calculator
For at beregne den energi, der kræves for at ændre et stofs temperatur:
Q =m × c × ΔT
Hvor Q is energy in joules, m is mass in kilograms, c er specifik varmekapacitet i Jkg⁻¹°C⁻¹ og ΔT er temperaturændringen i °C.
Varmefrigivet lommeregner – Eksempel
Antag, at 100 g af en syre blandes med 100 g af en base, hvilket hæver temperaturen fra 24°C til 32°C.
Neutraliseringsreaktionen kan forenkles til:
H⁺ + OH⁻ → H₂O
Beregninger:
- Masse:(100 g + 100 g) ÷ 1000 =0,2 kg
- Specifik varmekapacitet for vand:4.186 Jkg⁻¹°C⁻¹
- ΔT:32°C – 24°C =8°C
- Q =0,2 kg × 4.186 Jkg⁻¹°C⁻¹ × 8°C =6.688J
Thus, 6,688 joules of heat are released.
 Varme artikler
Varme artikler
-
 Elektrisk åle-inspireret enhed når 110 voltElektrisk ål-inspireret enhed når 110 volt:Dette billede viser den trykte, højspændingsimplementering af det kunstige elektriske organ. En 3-D bioprinter blev brugt til at afsætte arrays af gelprecurs
Elektrisk åle-inspireret enhed når 110 voltElektrisk ål-inspireret enhed når 110 volt:Dette billede viser den trykte, højspændingsimplementering af det kunstige elektriske organ. En 3-D bioprinter blev brugt til at afsætte arrays af gelprecurs -
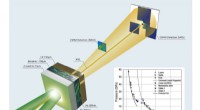 En stødinduceret mekanisme til oprettelse af organiske molekylerEksperimentel konfiguration af laserdrevne chokkomprimeringsforsøg på benzen. Kredit:Los Alamos National Laboratory Komplekse kulstofbaserede molekyler er overalt i kosmos. Hvor mange af disse mol
En stødinduceret mekanisme til oprettelse af organiske molekylerEksperimentel konfiguration af laserdrevne chokkomprimeringsforsøg på benzen. Kredit:Los Alamos National Laboratory Komplekse kulstofbaserede molekyler er overalt i kosmos. Hvor mange af disse mol -
 Materialer til brintservice avanceret af nyt multilab-konsortiumBrendan Davis, hoveddesigner og operatør af højtryksmekaniske testsystemer i Hydrogen Effects on Materials Laboratory ved Sandia National Laboratories, udarbejder et system til test med brintgas. Kred
Materialer til brintservice avanceret af nyt multilab-konsortiumBrendan Davis, hoveddesigner og operatør af højtryksmekaniske testsystemer i Hydrogen Effects on Materials Laboratory ved Sandia National Laboratories, udarbejder et system til test med brintgas. Kred -
 Ny kemisk modifikation af en naturlig forbindelse til kræftbehandlingGonçalo Bernardes, Principal Investigator ved iMM og medleder af undersøgelsen. Kredit:Gonçalo Ribeiro, iMM Naturlige forbindelser har ofte et lovende terapeutisk potentiale, men at bruge dem til a
Ny kemisk modifikation af en naturlig forbindelse til kræftbehandlingGonçalo Bernardes, Principal Investigator ved iMM og medleder af undersøgelsen. Kredit:Gonçalo Ribeiro, iMM Naturlige forbindelser har ofte et lovende terapeutisk potentiale, men at bruge dem til a
- Top EPA-rådgivere udfordrer mangeårig luftforureningsvidenskab, truer amerikanernes helbred
- Hvordan detailhandelskonkurrencen mellem CBD'er, indkøbscentre og online vil omforme vores byer
- Holder den europæiske avnbøg-plante bladene hele vinteren ligesom pyramideeg?
- Hvorfor ser det ud til, at himmellegemer bevæger sig fra østvest over himlen?
- Seks ting at vide om Florida red tide
- Bayer bekræfter prognoserne, efterhånden som Monsanto-integrationen skrider frem


