Hvilke faktorer driver hastigheden af en kemisk reaktion? En praktisk guide
MadamLead/iStock/GettyImages
En kemisk reaktion fortsætter, når reaktantmolekyler kolliderer med den korrekte orientering og tilstrækkelig kinetisk energi. Sandsynligheden for sådanne produktive kollisioner – og dermed reaktionshastigheden – er styret af flere nøglefaktorer.
Nøgledeterminanter for reaktionshastighed
1. Reaktantkoncentration
Højere koncentrationer øger frekvensen af kollisioner pr. tidsenhed, hvilket øger sandsynligheden for, at en kollision vil have den rigtige energi og orientering. Empirisk skalerer reaktionshastigheden ofte med koncentration efter hastighedsloven afledt af kollisionsteori.
2. Temperatur
Temperatur hæver den gennemsnitlige kinetiske energi af molekyler. Ifølge Arrhenius-ligningen kan en beskeden temperaturstigning eksponentielt øge hastighedskonstanten, efterhånden som flere molekyler overskrider aktiveringsenergitærsklen.
3. Tryk
For gasformige reaktanter reducerer komprimering af systemet den gennemsnitlige intermolekylære afstand og øger derved kollisionsfrekvensen. Forholdet er lineært for ideelle gasser (hastighed ∝ tryk), men kan afvige under ikke-ideelle forhold.
4. Overfladeareal
Reaktioner, der involverer en fast fase, har gavn af en større eksponeret overflade. Fine pulvere giver et større grænsefladeareal, forkorter diffusionsveje for reaktanter og accelererer reaktionen.
5. Fasekompatibilitet
Reaktanter, der deler den samme fase - både væsker, begge gasser eller begge faste stoffer - interagerer lettere. En fasemismatch (f.eks. fast-gas) reducerer sandsynligheden for kollisioner, fordi kun en delmængde af molekyler kan nå grænsefladen.
6. Katalysatorer
Katalysatorer sænker den aktiveringsenergi, der kræves til overgangstilstanden uden at blive forbrugt, hvilket øger reaktionshastigheden. I biologiske systemer muliggør enzymer - proteinkatalysatorer - processer, der ellers ville forløbe for langsomt for livet.
TL;DR
Rate ↑ med:højere koncentration, højere temperatur, højere tryk, større overfladeareal, katalysatorer og sammefasereaktanter.
Rate ↓ med:lavere koncentration, lavere temperatur, lavere tryk, reduceret overfladeareal, fraværende katalysatorer eller faseinkompatibilitet.
Sidste artikelMolekylvægt vs. molær masse:Hvad du behøver at vide
Næste artikelSådan beregnes varme frigivet i eksoterme reaktioner
 Varme artikler
Varme artikler
-
 Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m
Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m -
 Forskere finder en måde at skabe lang levetid, hurtigopladelige batterierKredit:CC0 Public Domain En gruppe forskere under ledelse af Skoltech -professor Pavel Troshin undersøgte koordineringspolymerer, en klasse af forbindelser, der næsten ikke er undersøgt i metalion
Forskere finder en måde at skabe lang levetid, hurtigopladelige batterierKredit:CC0 Public Domain En gruppe forskere under ledelse af Skoltech -professor Pavel Troshin undersøgte koordineringspolymerer, en klasse af forbindelser, der næsten ikke er undersøgt i metalion -
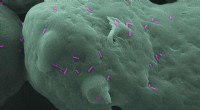 Forskere skaber 3-D-printede dele, der kan dræbe bakterierIndividuelle bakterier på en nylon-12 overflade. Bakterien er Pseudomonas aeruginosa, som kan forårsage sygdom hos planter, dyr og mennesker. Kredit:University of Sheffield Forskere fra University
Forskere skaber 3-D-printede dele, der kan dræbe bakterierIndividuelle bakterier på en nylon-12 overflade. Bakterien er Pseudomonas aeruginosa, som kan forårsage sygdom hos planter, dyr og mennesker. Kredit:University of Sheffield Forskere fra University -
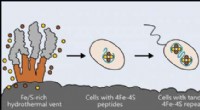 Forskere identificerer oprindelsen af metabolismeLivet kan være opstået i nærheden af hydrotermiske ventilationsåbninger rige på jern og svovl. De tidligste celler inkorporerede disse elementer i små peptider, som blev de første og enkleste ferred
Forskere identificerer oprindelsen af metabolismeLivet kan være opstået i nærheden af hydrotermiske ventilationsåbninger rige på jern og svovl. De tidligste celler inkorporerede disse elementer i små peptider, som blev de første og enkleste ferred
- Regulering af den indirekte arealanvendelse af kulstofemissioner fra biobrændstoffer påfører bræ…
- Hvordan metabolisk omprogrammering i mitokondrier fremmer eller underminerer overlevelse og lang lev…
- Hvilken videnskabsmand viste, at organismer ikke vokser i oksekød bouillon?
- Hvad er den opadgående kraft, der virker på vingen af et fly under flyvning?
- Grundforskning til verdensforandrende applikationer kan tage 6 måneder – eller 50 år
- Ford forventer et tab på 112 mio. USD i fjerde kvartal midt i omstruktureringsomkostninger


