Molekylvægt vs. molær masse:Hvad du behøver at vide
Af Riti Gupta
Opdateret 30. august 2022
Dizzy/iStock/GettyImages
Når man arbejder i kemi, skelnes der mellem molekylvægt og molær masse rejser ofte både studerende og fagfolk. Forskellen er udelukkende en af skala og enheder, men den er afgørende for nøjagtige beregninger i både laboratoriet og industrien.
Forstå det grundlæggende:Molecule vs Mole
Et molekyle er den mindste partikel af et stof, der stadig bevarer sin kemiske identitet. For eksempel indeholder et enkelt kuldioxidmolekyle (CO2) et kulstofatom og to oxygenatomer; nedbryde det yderligere, og det er ikke længere CO₂.
En muldvarp (mol) er en enhed, der repræsenterer et fast antal enheder - Avogadros tal, 6,022×10²³. Det er en bekvem måde at tælle atomer, molekyler eller andre diskrete partikler på. Således indeholder ét mol CO₂ 6,022×10²³ CO₂-molekyler.
Hvad er molekylvægt?
Molekylvægt er massen af et enkelt molekyle udtrykt i atomare masseenheder (amu). Det beregnes ved at summere atomvægtene af alle atomer i molekylet.
Eksempel:Vand (H₂O)
• Brint:1,008 amu
• Ilt:16.00amu
\(\text{Molekylvægt} =2(1,008\,\text{amu}) + 16,00\,\text{amu} =18,02\,\text{amu}\)
Hvad er molær masse?
Molær masse er massen af et mol af et stof og udtrykkes i gram pr. mol (g/mol). Det er numerisk lig med molekylvægten, men bruger en anden enhed til at afspejle den større skala.
Eksempel:Vand (H₂O)
• Brint:1,008g/mol
• Ilt:16,00g/mol
\(\tekst{Molar masse} =2(1,008\,\tekst{g/mol}) + 16,00\,\tekst{g/mol} =18,02\,\tekst{g/mol}\)
TL;DR
Molekylvægt =massen af et molekyle (amu). Molær masse =massen af et mol af det pågældende stof (g/mol). De numeriske værdier er identiske; enhederne er forskellige.
 Varme artikler
Varme artikler
-
 Forskere udvikler nye metoder til at studere materialer i mindst mulig skalaKredit: Videnskabens fremskridt Forskere over hele verden er interesserede i at udvikle nye materialer til at hjælpe mennesker med at leve mere bæredygtige og sunde liv, men stræben efter at prod
Forskere udvikler nye metoder til at studere materialer i mindst mulig skalaKredit: Videnskabens fremskridt Forskere over hele verden er interesserede i at udvikle nye materialer til at hjælpe mennesker med at leve mere bæredygtige og sunde liv, men stræben efter at prod -
 Et nyt peptid til hurtigt at dræbe multiresistente bakterierKonfokalmikroskopibillede af en klynge af A. baumannii-celler. Omega76 er farvet grøn, og ses interagere med membranen. Kredit:Indian Institute of Science Forskere ved Indian Institute of Science
Et nyt peptid til hurtigt at dræbe multiresistente bakterierKonfokalmikroskopibillede af en klynge af A. baumannii-celler. Omega76 er farvet grøn, og ses interagere med membranen. Kredit:Indian Institute of Science Forskere ved Indian Institute of Science -
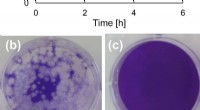 En materialevidenskabelig tilgang til bekæmpelse af coronavirus(a) Antiviral aktivitet af tilberedte pulvere mod coronavirus og fotografier, der viser ændringen i plaqueantal af coronavirus efter fire timer:(b) kontrol og (c) med CMO. Kredit:Materialebreve Fo
En materialevidenskabelig tilgang til bekæmpelse af coronavirus(a) Antiviral aktivitet af tilberedte pulvere mod coronavirus og fotografier, der viser ændringen i plaqueantal af coronavirus efter fire timer:(b) kontrol og (c) med CMO. Kredit:Materialebreve Fo -
 Team fremstiller magneter udelukkende af sjældne jordarter fra USACMI-forsker Ikenna Nlebedim har prøver af neodym-jern-bor-magneter, der er hentet og fremstillet udelukkende i USA. Evnen til at producere sjældne jordarters magneter på hjemmemarkedet kunne give posi
Team fremstiller magneter udelukkende af sjældne jordarter fra USACMI-forsker Ikenna Nlebedim har prøver af neodym-jern-bor-magneter, der er hentet og fremstillet udelukkende i USA. Evnen til at producere sjældne jordarters magneter på hjemmemarkedet kunne give posi
- Er skifer et element eller forbindelse?
- Hvad er den fjerde bevægelsesligning?
- Hvad kunne der ske i den fremtidige udvikling af nanovidenskab?
- Er den tid det tager for en fuld vibration af en partikel i medium?
- Eyes in the sky-projektet vil vise kraftværkets forureningsmærker
- Biomanipuleret enzym skaber naturlig vanillin fra planter i ét trin


