Forstå pH-skalaen:Hvordan surhedsgrad måles, og hvorfor det betyder noget
Af Kevin Beck Opdateret 30. august 2022
fotokostic/iStock/GettyImages
Selv de mest videnskabsvillige blandt os støder på udtrykket "pH" i hverdagen – lige fra shampooannoncer til dit hjemmeakvarium. pH-skalaen er et kemikers værktøj til at kvantificere, hvor sur eller basisk en opløsning er, og den er uundværlig inden for områder lige fra medicinsk diagnostik til miljøovervågning.
Hvad er pH-skalaen?
Forkortelsen pH står for "potentiale for hydrogenion". Dansk biokemiker Søren Sørensen opfandt udtrykket i 1909 og definerede det som den negative base-10-logaritme af hydrogen-ion-koncentrationen, [H⁺] . Matematisk:
pH = -\log₁₀[H⁺]
Dette logaritmiske forhold betyder, at hver enhedsændring på skalaen svarer til en ti-fold ændring i [H⁺]. En opløsning med en pH-værdi på 5,0 indeholder ti gange så mange hydrogenioner som én med en pH-værdi på 6,0.
Hvad er muldvarpe og molaritet?
I kemi bestemmer antallet af partikler - ikke deres masse - reaktiviteten. En muldvarp er lig med Avogadros antal (6,02×10²³) af enheder. Molmassen af et grundstof, der er angivet i dets periodiske "boks", fortæller, hvor mange gram en mol vejer.
For eksempel har natriumchlorid (NaCl) en molær masse på 58,5 g/mol. Opløsning af 5,85 g NaCl i 1 L vand giver en 0,10 M opløsning:
5.85 g ÷ 58.5 g/mol = 0.10 mol
En sådan koncentration svarer til 0,10 molL⁻¹ af opløste ioner.
Hvordan fungerer den logaritmiske skala?
En logaritme komprimerer brede numeriske områder til håndterbare værdier. I pH-sammenhæng ændrer hvert årti (faktor på ti) i hydrogen-ion-koncentration pH-værdien med en heltalsenhed. Denne skala er grunden til, at en "neutral" pH på 7 indikerer, at [H⁺] er lig med [OH⁻] i rent vand.
- Syrestyrke (kemikaliets iboende evne til at donere protoner) og syrekoncentration (hvor meget der er til stede) bestemmer tilsammen en opløsnings pH.
Måling af pH i praksis
Laboratorie-pH-målere bruger en glaselektrode, der reagerer på potentialforskellen mellem testopløsningen og en 1M hydrogen-ion-reference. Elektrodens spænding omdannes til en pH-værdi via kalibreringskurver.
Hvorfor pH betyder noget
Typiske pH-værdier illustrerer dens betydning:
- Mavesyre:~1,5
- Limesaft:~2,0
- Vin:~3,5
- Rent vand:7,0
- Menneskeblod:~7,4
- Blegemiddel:~9.0
- Hustandsammoniak:~12,0
Blod indeholder bicarbonat (HCO₃⁻), en naturlig buffer, der neutraliserer overskydende H⁺-ioner og holder pH-værdien tæt på 7,4. Antacida, som accepterer protoner, mindsker mavesyreindholdet ved at danne vandmolekyler fra hydroxylgrupper.
Prøve pH-beregninger
Eksempel 1: Hvad er pH-værdien af en opløsning med [H⁺] =4,9×10⁻⁷M?
pH=−log₁₀(4,9×10⁻⁷)=6,31
Eksempel 2: Hvad er [H⁺] i en opløsning med pH=8,45?
8,45=−log₁₀[H⁺]⇒[H⁺]=10⁻⁸.⁴⁵=3,5×10⁻⁹M
Interaktiv pH-beregner
Brug online pH-beregneren at udforske, hvordan syreidentitet og koncentration påvirker pH. Eksperimenter med forskellige syrer i rullemenuen og observer, hvordan en svagere syre ved en højere molaritet kan give en lavere pH end en fortyndet stærk syre.
 Varme artikler
Varme artikler
-
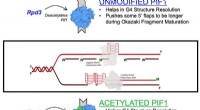 Kræftforbundet enzymmekanisme, der er nyligt karakteriseret i undersøgelseEt diagram, der illustrerer acetylering af Pif1-helicase-enzymet Kredit:Matthew Bochman og Lata Balakrishnan, Indiana University Bloomington/IUPUI En ny undersøgelse ledet af forskere ved IUPUI og
Kræftforbundet enzymmekanisme, der er nyligt karakteriseret i undersøgelseEt diagram, der illustrerer acetylering af Pif1-helicase-enzymet Kredit:Matthew Bochman og Lata Balakrishnan, Indiana University Bloomington/IUPUI En ny undersøgelse ledet af forskere ved IUPUI og -
 Nogle kan lide det kryogentGengivelse af First Element Fuels flydende brintstofpumpe til detailhandel. Pumpen indeholder en baldakin på toppen, og brændstoflageret er afbildet på bagsiden. Kredit:First Element Fuel Sandia N
Nogle kan lide det kryogentGengivelse af First Element Fuels flydende brintstofpumpe til detailhandel. Pumpen indeholder en baldakin på toppen, og brændstoflageret er afbildet på bagsiden. Kredit:First Element Fuel Sandia N -
 Hvordan man kombinerer elementer for at danne forbindelser:En praktisk vejledningAf Mara Pesacreta Opdateret 30. august 2022 Jeffrey Rasmussen/iStock/GettyImages At forstå, hvordan grundstoffer fra det periodiske system forenes for at skabe forbindelser, er grundlæggende for ke
Hvordan man kombinerer elementer for at danne forbindelser:En praktisk vejledningAf Mara Pesacreta Opdateret 30. august 2022 Jeffrey Rasmussen/iStock/GettyImages At forstå, hvordan grundstoffer fra det periodiske system forenes for at skabe forbindelser, er grundlæggende for ke -
 Hydrogenbindinger opdaget direkte for første gangEn hydrogenbinding dannes mellem en propellan (lavere molekyle) og den kuliltefunktionaliserede spids af et atomkraftmikroskop. De målte kræfter og afstanden mellem iltatomet ved AFM-spidsen og propel
Hydrogenbindinger opdaget direkte for første gangEn hydrogenbinding dannes mellem en propellan (lavere molekyle) og den kuliltefunktionaliserede spids af et atomkraftmikroskop. De målte kræfter og afstanden mellem iltatomet ved AFM-spidsen og propel
- Forudsige, hvad der kan ske med en dyrecelle, hvis du putter den i destilleret vand?
- Hvad reflekterer månen over?
- Hvilket træk ved overfladen blev forårsaget af erosion?
- Fælles syrebaseindikatorer
- Klima og vand i et foranderligt Afrika
- Hvad er atomnummeret, og hvad fortæller det dig om protoner i et atom?


