Polære vs. ikke-polære bindinger:Hvordan elektronegativitet former kemiske egenskaber
Af Riti GuptaOpdateret 30. august 2022
JK1991/iStock/GettyImages
Elektronegativitet er den drivkraft, der bestemmer, hvor stærkt et atom tiltrækker elektroner. Jo større et atoms elektronegativitet, jo mere trækker det delte elektroner mod sig selv. Dette princip understøtter de mange forskellige kemiske bindinger, vi støder på.
Når et atom er markant mere elektronegativt end dets partner, opstår der to scenarier. Det kan fuldstændigt fange en elektron fra det andet atom og danne en ionisk binding . Alternativt kan den blot trække de delte elektroner tættere på og skabe en polær kovalent binding . Bindinger, der involverer stærkt elektronegative atomer, såsom oxygen eller fluor, udviser typisk denne polære karakter, hvor det elektronegative atom bærer en delvis negativ ladning (δ‑) og dets partner en delvis positiv ladning (δ+).
Klassificering af kemiske bindinger
Obligationer falder langs et spektrum fra rent upolære til fuldt polære. En ionbinding repræsenterer det ekstreme, hvor et atoms elektronegativitetsforskel er så stor, at den tager en elektron helt. En ikke-polær kovalent binding opstår, når de to atomer deler elektroner ligeligt, som det ses i homonukleære diatomiske molekyler som H₂ eller Cl₂.
For bindinger, der ligger mellem disse yderpunkter, dikterer forskellen i elektronegativitet (ΔEN) bindingstypen. Følgende tabel opsummerer de almindeligt accepterede tærskler:
Bestemmelse af bindingstype baseret på forskel i elektronegativitet
| Obligationstype | Elektronegativitetsforskel (ΔEN) |
|---|---|
| Ren kovalent | < 0.4 |
| Polær kovalent | 0,4 – 1,8 |
| Ionisk | > 1.8 |
Forskellen mellem polære og upolære bindinger afhænger således af ΔEN.
Polære vs. ikke-polære molekyler
Et molekyle kan indeholde polære kovalente bindinger, men alligevel forblive upolære, hvis bindingsdipolerne ophæver hinanden på grund af molekylær symmetri. Vand (H₂O) er en klassisk polær forbindelse:dens bøjede geometri efterlader en nettodipol, hvilket muliggør omfattende hydrogenbinding. I modsætning hertil har bortrifluorid (BF₃) tre polære B-F-bindinger arrangeret i en plan trigonal form, der udligner, hvilket gør molekylet generelt upolært.
Hvorfor polaritet betyder noget
Polaritet har dybt indflydelse på, hvordan molekyler interagerer, især i opløsning. For eksempel opløses sukkerarter let i vand, fordi begge molekyler har polære funktionelle grupper, der danner hydrogenbindinger. Vandets oxygenatom bærer en delvis negativ ladning, mens brintatomerne bærer delvise positive ladninger, hvilket skaber et miljø, der favoriserer hydrogenbinding med sukkerets hydroxylgrupper (–OH).
Omvendt består olier stort set af ikke-polære CH-bindinger. Den lille elektronegativitetsforskel mellem kulstof og brint resulterer i ubetydelige dipolmomenter, hvilket forhindrer hydrogenbinding. Oliemolekyler interagerer således ikke positivt med vands polære netværk, hvilket fører til ublandbarhed.
Ved at undersøge en forbindelses strukturelle egenskaber og arten af dens bindinger kan kemikere forudsige, om den vil udvise polaritet og følgelig dens adfærd i forskellige kemiske sammenhænge.
 Varme artikler
Varme artikler
-
 Syre-basetitrering:Almindelige fejlkilder og hvordan man minimerer demAf Jack Brubaker | Opdateret 30. august 2022 I analytisk kemi er titrering fortsat en hjørnestensteknik til kvantificering af syrer og baser. En lille prøve af eddike, for eksempel, kan vurderes nøja
Syre-basetitrering:Almindelige fejlkilder og hvordan man minimerer demAf Jack Brubaker | Opdateret 30. august 2022 I analytisk kemi er titrering fortsat en hjørnestensteknik til kvantificering af syrer og baser. En lille prøve af eddike, for eksempel, kan vurderes nøja -
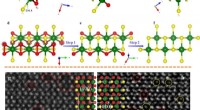 Kontrollerbar overfladedefektteknik på overgangsmetaltrichalcogenidFigur (a-f) viser den skematiske proces for omdannelsen af monoklint zirconiumtrisulfid, ZrS3 (ICCD PDF nr. 30-1498) til sekskantet zirconiumsulfid, ZrS2 (ICCD PDF-nr. 11-0679) fra [010] (a-c) og [0
Kontrollerbar overfladedefektteknik på overgangsmetaltrichalcogenidFigur (a-f) viser den skematiske proces for omdannelsen af monoklint zirconiumtrisulfid, ZrS3 (ICCD PDF nr. 30-1498) til sekskantet zirconiumsulfid, ZrS2 (ICCD PDF-nr. 11-0679) fra [010] (a-c) og [0 -
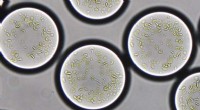 Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e
Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e -
 Ny bioinspireret lim binder enhver overflade under vandetKredit:Wageningen University &Research Undervandsadhæsion er teknisk udfordrende på grund af tilstedeværelsen af vand, den værste fjende for enhver lim. Nu, forskere fra Wageningen University &R
Ny bioinspireret lim binder enhver overflade under vandetKredit:Wageningen University &Research Undervandsadhæsion er teknisk udfordrende på grund af tilstedeværelsen af vand, den værste fjende for enhver lim. Nu, forskere fra Wageningen University &R
- Kan frugter lave elektricitet?
- Små huse lokker budgetbevidste amerikanere
- Hvad er ment ved at beskrive to egenskaber af?
- Generering af strøm fra forurenet luft
- Undersøgelse finder direkte forbindelser mellem gammelt kulstof, grafit og havbunden hydrotermiske …
- Hvad er 34 grader Celsius lig med i Fahrenheit?


