Hvordan man kombinerer elementer for at danne forbindelser:En praktisk vejledning
Af Mara Pesacreta
Opdateret 30. august 2022
Jeffrey Rasmussen/iStock/GettyImages
At forstå, hvordan grundstoffer fra det periodiske system forenes for at skabe forbindelser, er grundlæggende for kemi. Hvert elements unikke egenskaber styrer, hvordan det binder, uanset om det er gennem metalliske, ioniske eller kovalente interaktioner. At mestre disse principper gør det muligt for kemikere at forudsige og manipulere stoffers adfærd på tværs af videnskabelige og industrielle sammenhænge.
Trin 1:Identificer metaller, ikke-metaller og metalloider
Metaller optager venstre og midten af det periodiske system og udmærker sig som elektriske ledere - kobber er et klassisk eksempel. Metalloider såsom bor, silicium, germanium, arsen, antimon, tellur og polonium udviser blandede egenskaber, der bygger bro mellem metallisk og ikke-metallisk adfærd. Ikke-metaller, der findes på højre side (undtagen brint), har tendens til at være gasser eller sprøde faste stoffer og leder elektricitet dårligt; nitrogen eksemplificerer denne gruppe.
Trin 2:Genkend metallisk limning
Når identiske metalatomer kombineres, danner de metalbindinger. I dette arrangement er valenselektroner delokaliseret over et gitter, hvilket muliggør fri elektronstrøm – zink demonstrerer dette fænomen.
Trin 3:Overvej elementer med høj elektronegativitet
Halogener i Group17 har syv valenselektroner, hvilket gør dem meget elektronegative. Deres stærke tiltrækning af elektroner driver dannelsen af ioniske eller kovalente bindinger afhængigt af partnerelementet.
Trin 4:Overvej elementer med lav elektronegativitet
Alkalimetaller i gruppe 1 har en enkelt valenselektron, hvilket resulterer i de laveste elektronegativitetsværdier. Disse elementer donerer let elektroner under binding.
Trin 5:Metal-ikke-metal-interaktioner giver ioniske bindinger
Når et metal med lav elektronegativitet møder et ikke-metal med høj elektronegativitet, sker der elektronoverførsel, hvilket producerer et ionisk gitter. Kaliumchlorid (KCl) er et lærebogseksempel på en sådan forbindelse.
Trin 6:Ikke-metal-ikke-metalbindinger danner kovalente strukturer
Kombination af to eller flere ikke-metaller fører typisk til kovalente bindinger med delt elektron, som det ses i nitrogendioxid (NO₂). Disse molekyler udviser ofte retningsbestemt binding og defineret molekylær geometri.
Trin 7:Skeln mellem organiske og uorganiske forbindelser
Organisk kemi fokuserer på kulstofholdige molekyler. Methan (CH4) illustrerer en organisk forbindelse, hvorimod magnesiumbromid (MgBr₂) repræsenterer et rent uorganisk salt.
Værktøjer, du skal bruge
- Computer
- Kemi lærebog
- Periodisk tabelreference
- Pen
- Papir
 Varme artikler
Varme artikler
-
 Fysikere opdager en tri-anion partikel med kolossal stabilitetKredit:Virginia Commonwealth University Forskere fra Virginia Commonwealth University har opnået en bedrift, der er den første inden for fysik og kemi-en der kunne have vidtrækkende anvendelser.
Fysikere opdager en tri-anion partikel med kolossal stabilitetKredit:Virginia Commonwealth University Forskere fra Virginia Commonwealth University har opnået en bedrift, der er den første inden for fysik og kemi-en der kunne have vidtrækkende anvendelser. -
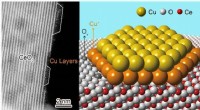 Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama
Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama -
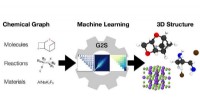 Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af
Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af -
 Beregning af molær koncentration:En trin-for-trin guideTotojang/iStock/GettyImages At kunne beregne koncentrationen af en opløsning er en af de mest basale færdigheder, der kræves af en videnskabsmand. Uden at vide, hvor meget af et stof du arbejder med,
Beregning af molær koncentration:En trin-for-trin guideTotojang/iStock/GettyImages At kunne beregne koncentrationen af en opløsning er en af de mest basale færdigheder, der kræves af en videnskabsmand. Uden at vide, hvor meget af et stof du arbejder med,
- Forståelse af polære kovalente bindinger:Ulige elektrondeling
- Hvordan kan kloratomer er i HCLO2?
- Hvordan man opbygger en model af en mini-basketballbane
- Kina fabrikker rationerer strøm, da hedebølgen sender efterspørgslen i vejret
- Saltsyre tilsættes til et bægerglas indeholdende et stykke zink. Det resulterer i, at chlorid dann…
- Hvad er et ord, der betyder kærlighed til naturen?


