Beregning af molær koncentration:En trin-for-trin guide
Totojang/iStock/GettyImages
At kunne beregne koncentrationen af en opløsning er en af de mest basale færdigheder, der kræves af en videnskabsmand. Uden at vide, hvor meget af et stof du arbejder med, har du ingen kontrol over de reaktioner, du udfører.
Koncentration af en løsning:Definition
Koncentration af en løsning:Definition
Koncentration af en opløsning angives primært i molaritet eller mol pr. liter. Forkortelsen for molaritet er M og koncentrationsenhederne er mol/L .
Definitionen af molaritet betyder, at man kan finde molariteten af en opløsning, hvis man kender det samlede antal mol af det opløste stof og det samlede volumen af opløsningen. Så for at beregne koncentrationen af en opløsning (i molaritet), skal du dividere mol opløst stof med det samlede volumen.
TL;DR (for lang; læste ikke)
Koncentrationsformel:For at finde den molære koncentration af en opløsning skal du blot dividere det samlede antal mol opløst stof med det samlede volumen af opløsningen i liter.
Beregning af en opløsnings molære koncentration
Beregning af en opløsnings molære koncentration
Lad os sige, at du har 10 mol NaCl, og dit samlede volumen af opløsning er 5 L. For at finde molariteten af denne opløsning skal du dividere det samlede antal mol opløst stof (NaCl) med det samlede volumen:
\(\mathrm{\dfrac{10mol\enspace NaCl}{5L}=2M\enspace NaCl}\)
Det betyder, at din 5 L opløsning, som indeholder 10 mol NaCl, er en 2 M NaCl-opløsning. Her siges "M" højt som "molar."
Hvad hvis du har en opløsning, der indeholder 10 gram NaCl i 5 L opløsning?
For at finde koncentrationen af denne nye opløsning skal du konvertere fra gram til mol . Dette kræver brug af molmassen (angivet i gram/mol) af NaCl. Molmassen af et stof findes ved at lægge molmassen af de enkelte komponenter sammen. For NaCl er de to komponenter natrium og chlorid.
For at finde molmassen af en af dem skal du kigge under deres symboler på det periodiske system. Den molære masse af natrium er 22,99 g/mol, og den molære masse af chlor er 35,45 g/mol. Tilføjet sammen giver dette dig den molære masse af NaCl, som er 58,44 g/mol.
Nu kan du finde koncentrationen af en 5 L opløsning, der indeholder 10 gram NaCl.
Begynd med at omdanne gram til mol:
\(\mathrm{ 10g\enspace NaCl\Biggl(\dfrac{1mol\enspace NaCl}{58.44g\enspace NaCl}\Biggr)=0,17mol\enspace NaCl}\)
Dernæst skal du dividere antallet af mol med det samlede volumen for at finde koncentrationen:
\(\mathrm{\dfrac{0,17mol\enspace NaCl}{5L}=0,034M\enspace NaCl}\)
Det betyder, at hvis du har 10 gram NaCl i en 5 L opløsning, vil du have en 0,034 M opløsning af NaCl.
Hvad hvis du har en opløsning, der indeholder 1.000 milligram NaCl i 5 L opløsning?
I dette tilfælde skal du først konvertere fra milligram til gram. Der er 1.000 milligram i 1 gram.
Så:
\(\mathrm{1000mg\enspace NaCl\Biggl(\dfrac{1g}{1000mg}\Biggr)=1g\enspace NaCl}\)
Nu hvor du ved, at 1.000 milligram svarer til 1 gram, kan du konvertere gram til mol ved hjælp af molmassen:
\(\mathrm{ 1g\enspace NaCl\Biggl(\dfrac{1mol\enspace NaCl}{58.44g\enspace NaCl}\Biggr)=0,017mol\enspace NaCl}\)
Til sidst kan du tage antallet af mol og dividere med det samlede volumen:
\(\mathrm{\dfrac{0,017mol\enspace NaCl}{5L}=0,0034M\enspace NaCl}\)
Således er 1.000 gram NaCl i 5 L total opløsning det samme som en 0,0034 M opløsning af NaCl.
Generelle ligninger til at finde koncentration
Generelle ligninger til at finde koncentration
Det følgende viser en generaliseret version af trinene vist ovenfor eller "koncentrationsformel ."
Givet mol opløst stof og liter opløsning beregnes molariteten ved:
\(\mathrm{\dfrac{mol\enspace solute}{L\enspace-løsning}=koncentration\enspace(M)}\)
Givet mængden af opløst stof i gram, giver følgende ligning koncentration:
\(\mathrm{g\enspace solute\Biggl(\dfrac{1mol\enspace solute}{molar\enspace masse\enspace of\enspace solute\enspace g}\Biggr)\Biggl(\dfrac{1}{L\enspace-løsning}\Biggr)=koncentration\enspace(M)}\)
Givet mængden af opløst stof i milligram, giver følgende ligning koncentration:
\(\mathrm{mg\enspace solute\Biggl(\dfrac{1g}{1000mg}\Biggr)\Biggl(\dfrac{1mol\enspace solute}{molar\enspace masse\enspace of\enspace solute\enspace g}\Biggr)\Biggl(\dfrac{1}{L\en løsning}\Biggr)=koncentration\enspace(M)}\)
 Varme artikler
Varme artikler
-
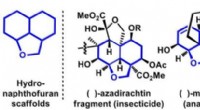 Vigtige tricykliske kemiske forbindelser med effektiv chiralitetskontrolFigur 1. Repræsentative eksempler på bioaktive molekyler med hydronaphthofurans stilladser. Kredit:Osaka University Osaka University-forskere udviklede en meget effektiv måde at producere chirale
Vigtige tricykliske kemiske forbindelser med effektiv chiralitetskontrolFigur 1. Repræsentative eksempler på bioaktive molekyler med hydronaphthofurans stilladser. Kredit:Osaka University Osaka University-forskere udviklede en meget effektiv måde at producere chirale -
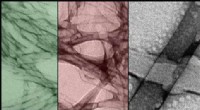 Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen -
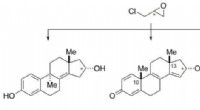 Forskere udvikler gennembrudsprocesser til at skabe kræft-dræbende lægemidlerEn ny kemisk vej fra simple kommercielt tilgængelige materialer til medicinsk-relevante molekyler. Kredit:Glenn Micalizio Et forskerhold ved Dartmouth College har udviklet en ny strategi for lægem
Forskere udvikler gennembrudsprocesser til at skabe kræft-dræbende lægemidlerEn ny kemisk vej fra simple kommercielt tilgængelige materialer til medicinsk-relevante molekyler. Kredit:Glenn Micalizio Et forskerhold ved Dartmouth College har udviklet en ny strategi for lægem -
 Overfladefugtelighed har ringe effekt på atmosfærisk vandopsamling, men kantstrukturen er afgøren…Vanddråber dannes på en overflade:kanten betyder mere end overfladens fugtighed. Kredit:KAUST Vandhøst er en ældgammel teknik til opsamling af atmosfærisk vanddamp. Forskere søger til naturen for
Overfladefugtelighed har ringe effekt på atmosfærisk vandopsamling, men kantstrukturen er afgøren…Vanddråber dannes på en overflade:kanten betyder mere end overfladens fugtighed. Kredit:KAUST Vandhøst er en ældgammel teknik til opsamling af atmosfærisk vanddamp. Forskere søger til naturen for
- Hvad er de gasser, der udvikles fra Na2CO3 plus HCL?
- Hvilken tilstand kan du finde det mest regnfulde sted på jorden?
- Hvordan dronningbier kontrollerer prinsesserne
- En ny ungarsk metode kan hjælpe proteinforskning
- Bjerge, der ligner dem i Grønland og Vesteuropa?
- NASAs Mars 2020 vil vise et spor for mennesker


